A adenomiose é uma patologia uterina bastante comum. Ocorre mais frequentemente na fase reprodutiva das mulheres e tende a desaparecer após a menopausa. No entanto, pode afetar mulheres de todas as idades e, na fase fértil, causar infertilidade. Tem como principal característica o crescimento de […]
A adenomiose é uma patologia uterina bastante comum. Ocorre mais frequentemente na fase reprodutiva das mulheres e tende a desaparecer após a menopausa. No entanto, pode afetar mulheres de todas as idades e, na fase fértil, causar infertilidade.
Tem como principal característica o crescimento de um tecido semelhante ao endométrio no miométrio. Ambas são camadas uterinas, fundamentais no processo gestacional.
O endométrio reveste internamente o útero e é preparado pela ação hormonal para receber o embrião a cada ciclo menstrual: é nessa camada que ele se implanta, sendo abrigado e nutrido até que a placenta seja formada.
Enquanto o miométrio, camada muscular intermediária, é responsável pelas contrações na hora do parto.
Ainda que represente risco para fertilidade e cause a manifestação de sintomas, a adenomiose pode ser controlada. O tratamento é realizado de acordo com o desejo da paciente: se pretende ou não engravidar no momento. Continue a leitura e saiba mais!
À medida que o tecido anormal se desenvolve no miométrio provoca um processo inflamatório e a formação de bolsas, que resultam na manifestação de diferentes sintomas, comprometendo, muitas vezes, a qualidade de vida das mulheres portadoras. Porém, em boa parte dos casos a adenomiose é assintomática ou manifesta apenas um desconforto leve.
Se houver a manifestação de qualquer um deles, individualmente ou em associação, um especialista deverá ser procurado. O diagnóstico precoce aumenta a eficácia do tratamento, assim como evita ou alivia os sintomas.
Embora a causa exata de adenomiose ainda permaneça desconhecida, algumas teorias explicam o desenvolvimento do tecido ectópico no miométrio. Sugerem, por exemplo, que ele pode ter sido depositado no miométrio durante a formação fetal ou provocadas por cirurgias, ou de o miométrio ser invadido por células-tronco da medula óssea.
A adenomiose é classificada como focal quando um ou mais focos estão localizados em diferentes pontos do miométrio e, como difusa, se estiver espalhada em maior quantidade pela camada muscular.
Adenomiose e endometriose são patologias uterinas frequentemente confundidas. No entanto, elas se diferenciam no local de implante do tecido ectópico. Na endometriose ele desenvolve fora da cavidade uterina, nos ovários ou tubas uterinas, por exemplo. Já na adenomiose os implantes são restritos ao miométrio. Ambos são dependentes de estrogênio, portanto normalmente diminuem após a menopausa, quando não há mais a produção desse hormônio.
Embora o risco de a doença provocar infertilidade fosse considerado raro até bem pouco tempo, diversos estudos atuais têm sugerido a interferência da adenomiose no processo reprodutivo, na gravidez espontânea ou realizada por técnicas de reprodução assistida. Veja abaixo o que eles explicam:
Além dos sintomas, a suspeita de adenomiose é inicialmente confirmada pelo exame físico, quando é possível perceber alterações como o aumento do volume uterino e maior sensibilidade à palpação.
Posteriormente são realizados exames de imagem para confirmar a presença do tecido anormal ou mesmo descartar a possibilidade de outras patologias uterinas, que podem causar sintomas semelhantes, como a endometriose, miomas uterinos ou pólipos endometriais.
A exclusão de outras patologias é, da mesma forma, importante para confirmar a possibilidade de adenomiose, uma vez que o diagnóstico definitivo só pode ser realizado quando há remoção de implante ectópico do miométrio por histeroscopia.
A adenomiose é uma doença crônica e o tratamento tem como finalidade aliviar os sintomas e aumentar as chances de gravidez, nos casos de infertilidade quando há o desejo de ter filhos.
Se a mulher não tem a intenção de engravidar, são prescritos analgésicos e anti-inflamatórios não esteroides (AINEs) para aliviar dor e inflamação e medicamentos hormonais para controlar o aumento do fluxo menstrual.
Para mulheres que pretendem engravidar ou manifestam sintomas mais severos, que interferem com a qualidade de vida, é indicada a cirurgia para a remoção do tecido ectópico. O objetivo é a eliminação por hemiablação endometrial, mas é apenas eficaz quando o tecido não penetrou o miométrio mais profundamente.
Nos casos em que já invadiu o miométrio ou se houver infertilidade e a adenomiose for o único fator, o tratamento mais indicado é a fertilização in vitro (FIV).
Para reduzir a inflamação e não causar interferências na implantação do embrião, antes de a mulher ser submetida ao tratamento, são prescritos medicamentos que bloqueiam os níveis hormonais e também melhoram a receptividade uterina.
Com essas medidas, há maiores chances de mulheres com adenomiose engravidarem.
Quando a gravidez é confirmada, há um acompanhamento de todo o processo gestacional. A adenomiose, entretanto, não representa nenhum risco à mãe ou ao feto.
Conheça tudo sobre adenomiose aqui.
MaisEste post aborda sobre um exame importante quando há dificuldades em engravidar: a histerossalpingografia.
Dois tubos com cerca de 10 cm localizados em cada lado do útero, as tubas uterinas compõem o sistema reprodutor feminino, assim como útero, ovários e vagina. São elas que conduzem o óvulo liberado pelos ovários e os espermatozoides para que ocorra a fecundação.
São divididas em quatro partes: uterina, istmo, ampola e infundíbulo. No infundíbulo, extremidade próxima aos ovários, as fimbrias, segmentos semelhantes à uma franja, movimentam e conduzem o óvulo para o interior das tubas, que viajam até a ampola, dilatação posterior ao istmo (porção medial): é a parte mais longa e geralmente onde ocorre a fecundação, quando os espermatozoides alcançam o óvulo.
A histerossalpingografia é o principal exame realizado para avaliar a função tubária. Isso se refere não somente à sua permeabilidade, como também à anatomia, por exemplo se é tortuosa, aderida ou semiobstruída. O fator tubário pode responder a cerca de 30% das causas de infertilidade feminina.
Continue a ler este texto e entenda tudo sobre o exame, do funcionamento e casos em que é indicado, às técnicas de reprodução.
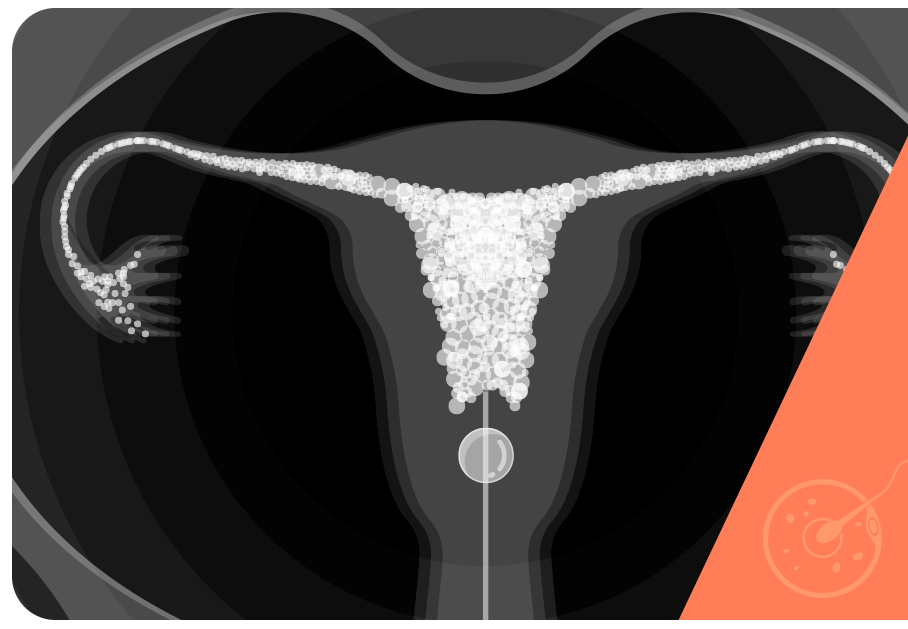
Histerossalpingografia (HSG) é um tipo de exame de raio-X com contraste iodado que permite a visualização da cavidade uterina e trompas, da mesma forma que é minimamente invasivo e considerado seguro à exposição por radiação.
Além de obstruções nas tubas uterinas, que dificultam a fecundação, o exame também é indicado se houver suspeita de anormalidades uterinas, congênitas ou provocadas por condições como pólipo e miomas uterinos, por exemplo: elas podem inibir o desenvolvimento da gravidez, levando, nesse caso, a abortamentos repetidos.
Ou seja, é particularmente indicado quando há suspeita de infertilidade feminina causada por esses fatores, além de sinequias, tumores uterinos e endometriose, ou mesmo para avaliar o resultado da cirurgia de esterilização feminina (laqueadura).
A histerossalpingografia pode ser realizada em ambiente ambulatorial, como clínicas de imagem. Após a injeção do contraste, a paciente é posicionada sob a máquina de raio-X e as imagens são feitas em diferentes posições: a fluoroscopia cria uma sequência e a projeta em uma tela. Ao final do exame, as sequências são armazenadas em diferentes mídias.
No entanto, alguns aspectos devem ser observados para a sua realização:
Os resultados da histerossalpingografia são fundamentais para a definição da abordagem de tratamento mais adequada a cada paciente: por cirurgia ou técnicas de reprodução assistida.
Obstruções podem ocorrer em apenas uma, ou em ambas (bilateral) as tubas. Por não provocarem sintomas na maioria dos casos, geralmente só são identificadas quando há dificuldades em engravidar.
Já a suspeita de anormalidades uterinas, surge a partir da detecção de patologias que podem provocá-las, ou quando ocorrem abortamentos consecutivos.
A obstrução pode ser tratada com cirurgia quando atinge seu terço médio ou distal. Nesse caso, muitas vezes a causa da obstrução são aderências que bloqueiam a tuba de forma extrínseca e ao serem desfeitas soluciona a obstrução, permitindo a passagem de óvulo e espermatozoides e, consequentemente, a fecundação.
As anormalidades uterinas também podem ser corrigidas por cirurgia, em ambos os casos as técnicas utilizadas são minimamente invasivas.
Nas obstruções tubárias proximais (istmo) ou em danos mais graves, que exigem a remoção de ambas as tubas, ainda é possível engravidar por tratamentos de reprodução assistida.
A técnica mais indicada para aumentar as chances de gravidez de mulheres com obstruções tubárias é a fertilização in vitro (FIV).
A FIV foi, inclusive, desenvolvida com este objetivo na década de 1970, momento em se tornou conhecida após o nascimento de Louise Brown, o primeiro bebê concebido com a sua utilização.
Prevê a fecundação de óvulos e espermatozoides em laboratório e, posteriormente, a transferência dos embriões formados nesse processo diretamente para o útero materno. Ou seja, as tubas uterinas não possuem nenhuma função.
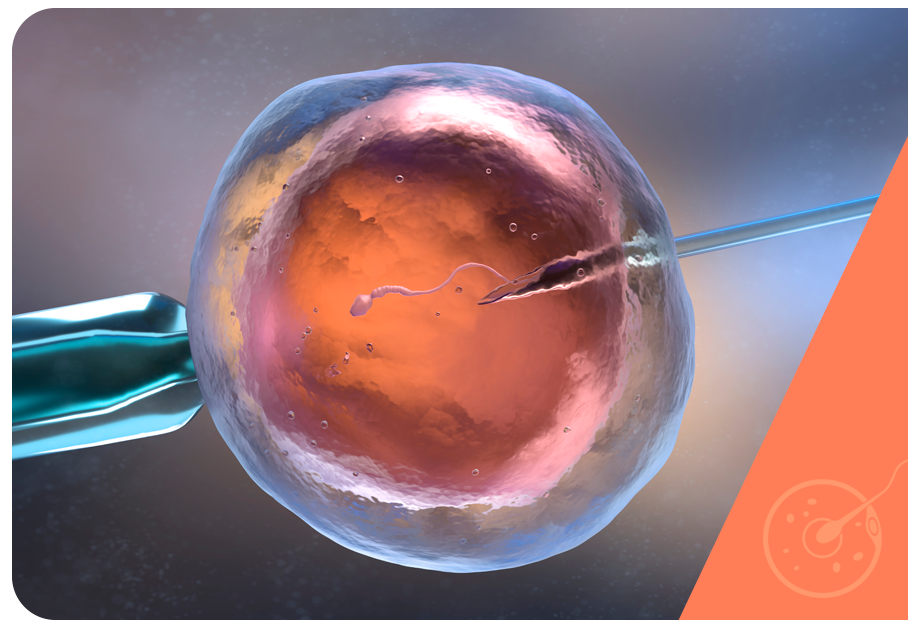
Atualmente o método mais utilizado para realizar a fecundação é a FIV com ICSI, ou injeção intracitoplasmática de espermatozoides incorporada ao tratamento em 1992: os espermatozoides são diretamente injetados em cada óvulo, aumentando, dessa forma, as chances de fecundação e a quantidade de embriões formados.
Além disso, reúne um conjunto de técnicas complementares, importantes para solucionar diversos problemas. Mulheres com distorções na anatomia uterina que não puderam ser corrigidas cirurgicamente, por exemplo, podem recorrer a uma delas para engravidar, o útero de substituição.
Após a fecundação, o útero pode ser cedido por parentes das pacientes em tratamento, como mães, irmãs, tias, sobrinhas e primas.
Os percentuais de sucesso gestacional da FIV por ciclo de são bastante expressivos: em média 50% quando se obtêm 2 bons embriões.
Siga o link e entenda detalhadamente o funcionamento da histerossalpingografia.
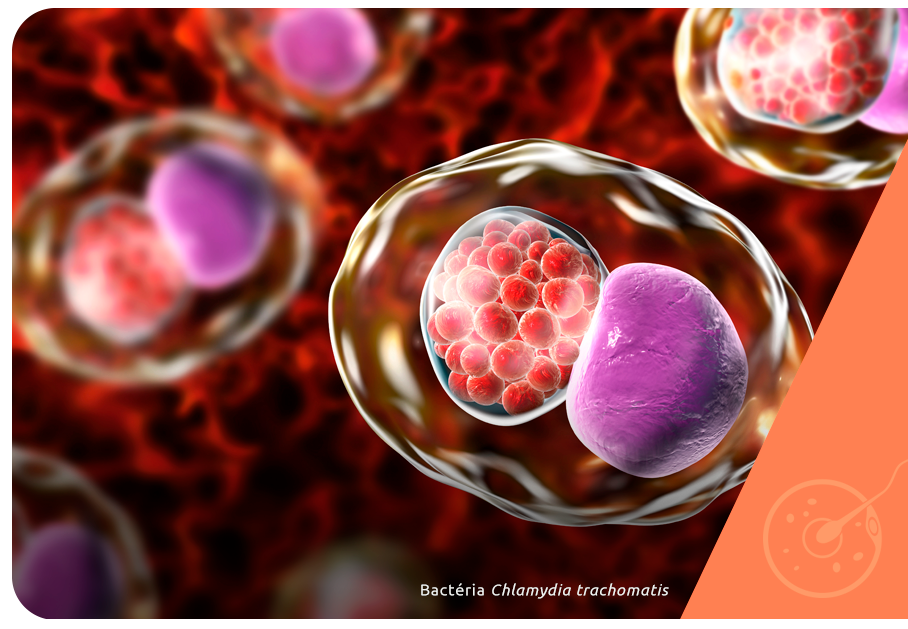
MaisA maioria das pessoas sexualmente ativas já ouviu falar em clamídia ou foi infectada pela bactéria Chlamydia trachomatis, uma vez que ela é uma das infecções sexualmente transmissíveis (IST) de maior incidência no mundo todo. A gonorreia, causada pela Neisseria gonorrhoeae também é conhecida e […]
A maioria das pessoas sexualmente ativas já ouviu falar em clamídia ou foi infectada pela bactéria Chlamydia trachomatis, uma vez que ela é uma das infecções sexualmente transmissíveis (IST) de maior incidência no mundo todo.
A gonorreia, causada pela Neisseria gonorrhoeae também é conhecida e é bastante comum as duas ocorrerem em associação.
Embora elas sejam a IST mais frequentemente registrada, outras, provocadas por bactérias, vírus ou protozoários, também podem afetar a saúde feminina e masculina, incluindo a reprodutiva, quando há prática sexual sem o uso de preservativos. Muitas vezes, inclusive, com risco de morte, como é o caso da sífilis em estágios mais avançados.
HPV (condiloma acuminado), herpes simples e tricomoníase compõem ainda a lista.
Continue a leitura e entenda tudo sobre a infecção por clamídia.
É difícil saber quem tem clamídia, pois geralmente as pessoas infectadas não apresentam nenhum sintoma. Assim, se torna facilmente disseminada. Para se ter uma ideia, cerca de 2 milhões de casos são registrados anualmente no Brasil.
A prevalência é maior entre as mulheres jovens, no entanto pode afetar homens e mulheres de qualquer idade, transmitida pelo sexo vaginal, oral ou anal desprotegido com pessoas infectadas. As mães podem, ainda, transmitir a bactéria para os filhos durante o parto.
No entanto, a clamídia é facilmente tratada quando é diagnosticada precocemente. As complicações, entre elas problemas de infertilidade, surgem apenas em estágios mais avançados da infecção. Veja abaixo as consequências em mulheres e homens:
A infecção por clamídia nos homens também pode evoluir para diferentes processos inflamatórios que comprometem a fertilidade:
A uretrite, inflamação da uretra, também pode ser consequência em mulheres e homens, ao mesmo tempo que a reincidência de clamídia aumenta o risco para ocorrência de HIV, vírus que provoca aids.
Ainda que a infecção por clamídia geralmente não provoque sintomas, em alguns casos eles podem manifestar e alertam para a necessidade de procurar auxílio médico.
Quando há sintomas, eles podem manifestar suavemente ou isoladamente. Nas mulheres os mais comuns são necessidade urgente e frequente de micção, corrimento vaginal anormal e com odor forte, sangramento em os períodos menstruais, dor abdominal e durante o sexo, inchaço da vagina e ao redor ânus e febre baixa.
Enquanto nos homens, além da urgência de micção, sensibilidade, inchaço e dor testicular, secreção peniana aquosa e leitosa, irritação ou sangramento no ânus, são os que geralmente manifestam.
Diagnóstico e tratamento de clamídia são bastante simples. O rastreio é feito pela análise das secreções ou por exame de sangue, que possibilitam a detecção da bactéria Chlamydia trachomatis. Nas mulheres, também pode ser identificada pelo Papanicolau de rotina.
O tratamento, por outro, prevê a prescrição de antibióticos. Parceiro ou parceira deverão ser tratados para evitar a reinfecção, que aumenta o risco de ocorrerem complicações. Durante o tratamento é importante não manter relações sexuais.
Para confirmar a cura é aconselhado a repetição do rastreio aproximadamente três meses após o início do tratamento. Se houver necessidade, o tratamento também deverá ser repetido.
Quando a clamídia provoca obstruções tubárias ou nos dutos que armazenam e transportam os espermatozoides a indicação de tratamento é a fertilização in vitro com injeção intracitoplasmática de espermatozoides (FIV com ICSI).
Na técnica, cada espermatozoide é avaliado individualmente e injetado diretamente no óvulo para que a fecundação ocorra. Os embriões formados são posteriormente transferidos para o útero. Assim, as tubas uterinas, onde a fecundação acontece na gestação natural, não têm nenhuma função.
Se o problema for a infertilidade masculina causada por obstruções ou ausência dos espermatozoides no sêmen, eles podem ser recuperados diretamente dos epidídimos ou testículos por diferentes abordagens cirúrgicas.
As chances de gravidez com a utilização da técnica são, em média, 40% a cada ciclo de realização do tratamento.
Gostou do texto e quer saber mais sobre a infecção por clamídia? Toque aqui.
MaisEmbora sejam formações benignas, os miomas uterinos podem causar infertilidade em alguns casos. Toque aqui e saiba mais.
A falta de sucesso em engravidar geralmente causa ansiedade e apreensão nas mulheres que estão tentando. No entanto, é normal a gravidez não ocorrer por até um ano de relações sexuais desprotegidas e frequentes.
Apenas após esse período pode haver suspeita de infertilidade. Nesse caso é importante procurar um especialista para investigar o que pode estar dificultando a concepção.
São várias as patologias femininas que podem causar alterações na fertilidade feminina durante a fase reprodutiva, entre elas estão alguns tipos de miomas.
A possibilidade de ter miomas assusta muitas mulheres. No entanto, embora eles sejam comuns e afetem um percentual significante das que estão vivenciando essa etapa, o índice de infertilidade, ao contrário, é bastante baixo.
Continue a leitura para saber mais como os miomas podem provocar infertilidade, os métodos diagnósticos e tratamento, incluindo as técnicas de reprodução assistida.
Miomas são tumores benignos que se desenvolvem na cavidade uterina e não estão associados ao câncer de útero, assim como é rara a possibilidade de se tornarem malignos.
O desenvolvimento deles pode ser provocado por diversos fatores, entretanto, a causa exata ainda é desconhecida. Estudos observaram, por exemplo, que o estrogênio e progesterona, hormônios sexuais femininos, que estimulam o espessamento do endométrio, camada que reveste internamente o útero, a cada mês, também são responsáveis pelo crescimento deles.
Genética e obesidade aumentam, da mesma forma, o risco. No primeiro caso a incidência em parentes de primeiro grau das mulheres portadoras, como mães ou irmãs, é frequentemente registrada, enquanto o sobrepeso responde por aproximadamente 20% dos casos.
Outro fator importante é a diferença racial: mulheres negras têm maior propensão para desenvolvê-los quando comparadas com as brancas. Assim como as que menstruaram precocemente.
Nem todo tipo de miomas causa infertilidade, as alterações ocorrem de acordo com o local de crescimento, critério que interfere, ao mesmo tempo, nos sintomas provocados por eles.
Os sintomas mais comuns de miomas uterinos são o aumento do fluxo menstrual, períodos mais longos do que o normal, cólicas severas durante os períodos ou sangramento anormal entre eles, além de micção frequente, sensação de pressão na parte inferior do abdome e dor durante a relação sexual (dispareunia).
Porém, como alguns são manifestações comuns a outras patologias uterinas, tentantes devem procurar um especialista para confirmar o problema.
O útero é formado por três camadas: endométrio, que o reveste internamente, miométrio, a camada muscular intermediária e perimétrio, a camada serosa exterior.
No endométrio o embrião implanta, é nutrido e fica abrigado até a formação da placenta. Os miomas que se desenvolvem nessa camada são chamados submucosos e, embora sejam o tipo menos comum, é o que mais causa alterações na fertilidade.
Eles afetam, por exemplo, a receptividade endometrial, fundamental para a implantação do embrião ser bem-sucedida. Assim, resulta em falhas e abortamento. Por outro lado, quando crescem próximos às tubas uterinas podem provocar obstrução, dificultando ou impedindo a fecundação.
Miomas submucosos que se estendem para o interior do útero, chamados intracavitários, tendem, ainda, a causar complicações na gravidez, incluindo descolamento da placenta, parto prematuro e hemorragia pós-parto, embora eles não provoquem nenhum risco para o desenvolvimento fetal.
O miométrio, camada intermediária e muscular, promove as contrações na hora do parto. Os miomas que crescem nessa camada são o tipo mais comum: é, inclusive, a partir de uma única célula do miométrio que eles se formam.
São chamados miomas intramurais e possuem tamanhos que variam de poucos milímetros a vários centímetros. Maiores, podem causar distorção na anatomia uterina dificultando o desenvolvimento do feto ou impedindo a sustentação da gravidez.
Sintomas como sangramento abundante ou entre os períodos e cólicas severas são característicos desses dois tipos de miomas.
Se crescerem no perimétrio, camada externa ou serosa, os miomas são chamados subserosos. Por terem mais espaço podem atingir grandes dimensões e comprimir órgão com a bexiga, levando ao aumento na frequência urinária e, do volume uterino. Porém, esse tipo de mioma não causa nenhuma alteração na fertilidade.
Ainda que possam resultar em infertilidade os miomas têm tratamento na maioria das vezes e uma grande parte das tentantes consegue engravidar quando eles são a única causa de infertilidade.
Além dos sintomas, a suspeita de miomas surge geralmente durante o exame ginecológico de rotina com a detecção de sinais como o aumento do volume uterino.
Para confirmar a presença de miomas e descartar a possibilidade de outras patologias uterinas que podem manifestar sintomas semelhantes, incluindo a endometriose e os pólipos endometriais, são realizados diferentes exames de imagem.
A partir dos resultados diagnósticos é definida a abordagem terapêutica mais adequada para cada paciente, que considera o desejo dela engravidar no momento e a severidade dos sintomas.
Quando os miomas não causam sintomas ou infertilidade, devem ser apenas observados. Se houver sintomas é indicada a terapia hormonal: ao mesmo tempo os alivia e contribui para a redução, também importante se houver necessidade de cirurgia.
A cirurgia tem como objetivo removê-los e é indicada para as mulheres com infertilidade que desejam engravidar, ou se os sintomas manifestarem de forma mais severa. O procedimento é conhecido como miomectomia e é realizado por técnicas minimamente invasivas. Nos casos em que os miomas resultam em distorção da anatomia uterina, ela também é corrigida.
Há boas chances de gravidez após o tratamento. Se isso não acontecer, como nos casos em que eles provocam obstruções ou anormalidades uterinas, a fertilização in vitro (FIV) é a técnica de reprodução assistida mais adequado quando a infertilidade provocada por miomas.
A FIV prevê a fecundação de óvulos e espermatozoides em laboratório e transferência dos embriões para o útero. Dessa forma, permite contornar as obstruções tubárias causadas por miomas intramurais, uma vez que não há função para as tubas uterinas.
Enquanto o teste ERA, uma das técnicas complementares à FIV, ajuda a identificar com o período mais provável de receptividade uterina para transferir o embrião. O teste contribui para minimizar as falhas de implantação e abortamento.
A FIV proporciona, em média, 50% de chance de a gravidez ser bem-sucedida a cada ciclo de tratamento quando se tem de 1 a 2 bons embriões.
Siga o link e entenda tudo sobre miomas uterinos.
MaisÉ no útero que o embrião implanta e desenvolve até o nascimento. O órgão, um dos mais importantes do sistema reprodutor feminino, é revestido por três camadas: endométrio, miométrio e perimétrio ou camada serosa. Duas delas, o endométrio e o miométrio, são particularmente importantes para […]
É no útero que o embrião implanta e desenvolve até o nascimento. O órgão, um dos mais importantes do sistema reprodutor feminino, é revestido por três camadas: endométrio, miométrio e perimétrio ou camada serosa. Duas delas, o endométrio e o miométrio, são particularmente importantes para a gravidez.
O endométrio, formado por tecido epitelial vascularizado, o reveste internamente. É nele que o embrião implanta e fica abrigado até que a placenta seja formada.
Miométrio é a camada intermediária, de musculatura lisa, com fibras que aumentam em quantidade e tamanho na hora do parto, permitindo, assim, as contrações.
Já o perimétrio é a mais externa e é formado principalmente por uma camada serosa, constituída de mesotélio e tecido conjuntivo.
A adenomiose ocorre quando o endométrio cresce na camada muscular (miométrio). Continue a leitura para entender melhor esta patologia uterina.
Apesar de não ser muito conhecida, a adenomiose é bastante comum e pode afetar uma em cada dez mulheres no mundo todo, de acordo com a Organização Mundial da Saúde (OMS). Por ser quase sempre assintomática geralmente é tardiamente diagnosticada e, com a progressão da doença, que causa a formação de pequenas bolsas no miométrio, os sintomas podem surgir de forma mais severa, comprometendo a qualidade de vida das mulheres portadoras.
No entanto, quando é diagnosticada precocemente, os sintomas podem ser evitados pela administração de medicamentos.
Até o momento não existe uma causa definida para o crescimento do tecido anormal no miométrio, mas estudos vêm demostrando que os receptores de hormônios esteroides sexuais, moléculas inflamatórias, enzimas da matriz extracelular e fatores de crescimento, por exemplo, desempenham um papel importante no seu surgimento.
De acordo com a teoria mais comum, a adenomiose resulta da invaginação do endométrio basal no miométrio através de uma zona juncional, limite entre o miométrio e o endométrio, alterada ou interrompida.
O que pode ser consequência de contrações miométricas, resultando em microtraumas contínuos à zona juncional, causando inflamação que, por sua vez, promove o aumento da dor e contração e por consequência mais inflamação, induzindo a um ciclo vicioso e mantido sob influência da ação hormonal de estrogênios.
Ou seja, a cada vez que ocorre a lesão ela é reparada e a continuidade leva à invasão de glândulas e estroma endometriais ao miométrio. Essa teoria apoia o entendimento comum de que a adenomiose está associada à multiparidade, à cesariana prévia e à cirurgia uterina prévia.
Outra teoria alternativa propõe que a doença surge a partir da metaplasia de células-tronco embrionárias ou adultas no miométrio, levando ao estabelecimento de novo tecido endometrial ectópico dentro da parede miometrial.
Por ser dependente de estrogênio, assim como outras patologias uterinas, geralmente retrocede na menopausa, período em que os níveis do hormônio são naturalmente muito baixos a ausentes. Além disso, a adenomiose é benigna e raramente afeta a fertilidade feminina.
Embora sempre tenha sido considerada uma condição clássica de mulheres multíparas acima de 40 anos com dor e sangramento menstrual intenso, o cenário epidemiológico mudou completamente. A adenomiose é cada vez mais identificada em mulheres jovens com dor e infertilidade ou nenhum sintoma. Geralmente é detectada por técnicas de imagem como a ultrassonografia transvaginal ou ressonância magnética (RM).
A relação com a infertilidade também é justificada por diferentes estudos. Eles sugerem, por exemplo, que a alteração na zona juncional pode causar falhas na implantação do embrião, na gravidez natural ou por fertilização in vitro (FIV), principalmente se forem muitos focos e de forma difusa no miométrio.
E ainda que as bolsas formadas no miométrio como consequência do processo inflamatório tendem a causar hipermobilidade uterina irregular, inibindo, dessa forma, o transporte de espermatozoides até as tubas uterinas e, consequentemente, a fecundação. A mobilidade do embrião também pode ser afetada, assim como a sua capacidade de implantação.
Mulheres afetadas por adenomiose podem apresentar sangramento uterino anormal, dismenorreia (cólicas severas), dispareunia (dor durante a relação sexual) ou infertilidade, mas um terço delas são assintomáticas. Em muitos casos, o sangramento pode ocorrer durante um tempo maior ou mesmo entre os períodos menstruais.
Um especialista deverá ser consultado quando os sintomas manifestarem por mais de dois meses consecutivos. Se for diagnosticada precocemente, as chances de serem aliviados por medicamentos são bem maiores.
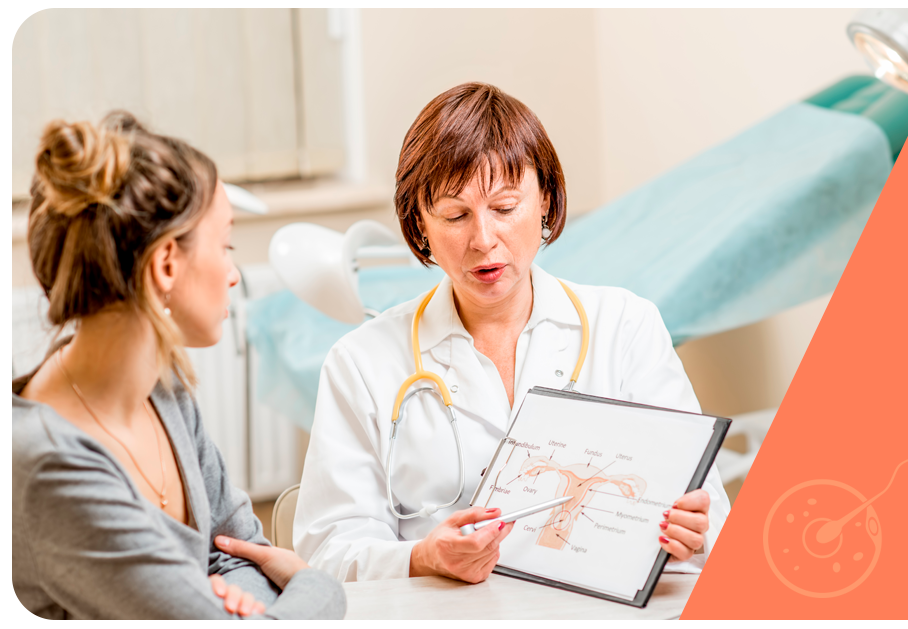
A evolução de técnicas de imagem, como ressonância magnética e ultrassonografia transvaginal, possibilitou um diagnóstico não invasivo de adenomiose. Entre as características que podem indicar a doença estão as alterações da zona juncional, como o espessamento, a presença de bolsas (cistos) no miométrio, assimetria da parede uterina e sombreamento do miométrio.
O tratamento tem como objetivo a redução dos sintomas provocados pela doença. Se a mulher não deseja engravidar, para controlar o fluxo menstrual abundante e cólicas severas, são prescritos medicamentos hormonais.
A cirurgia é indicada quando há o desejo de engravidar ou os sintomas impactarem a qualidade de vida. O objetivo é a eliminação do tecido ectópico por ablação endometrial por histeroscopia.
Se a mulher for infértil e a adenomiose a principal causa, a técnica mais indicada para aumentar as chances de gravidez é a FIV, considerada a mais eficiente entre os tratamentos de reprodução assistida, por possuir maiores índices de sucesso.
Antes, porém, os níveis hormonais são bloqueados por um período de dois a seis meses, causando, assim, uma redução da inflamação e, garantindo ao mesmo tempo, maior receptividade uterina.
Toque no link e saiba mais sobre adenomiose.
MaisA infertilidade é um problema comum a pessoas no mundo todo. Causada por diferentes doenças, geralmente assintomáticas, é descoberta muitas vezes quando há dificuldades para engravidar. Miomas uterinos, endometriose e doença inflamatórias pélvicas (DIPA), exemplos de patologias frequentemente registradas, que causam alterações na fertilidade feminina. […]
A infertilidade é um problema comum a pessoas no mundo todo. Causada por diferentes doenças, geralmente assintomáticas, é descoberta muitas vezes quando há dificuldades para engravidar.
Miomas uterinos, endometriose e doença inflamatórias pélvicas (DIPA), exemplos de patologias frequentemente registradas, que causam alterações na fertilidade feminina. Anormalidades uterinas, cisto ou tumores em ovários e distúrbios genéticos, também podem provocar o problema.
A complexidade e a ausência de sintomas dificultam o diagnóstico precoce o que aumenta ainda mais os danos provocados.
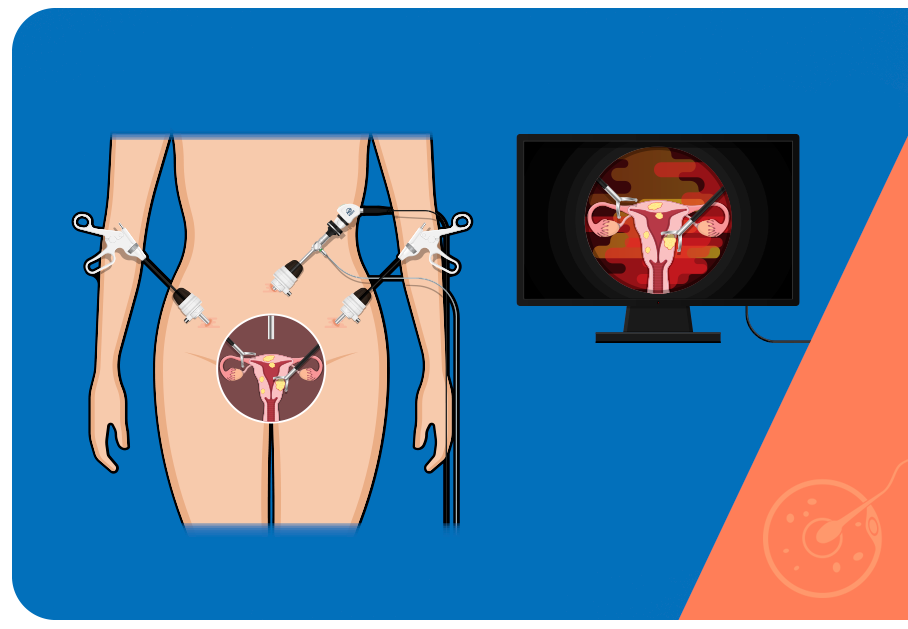
A videolaparoscopia, atualmente, tornou-se parte integrante da cirurgia ginecológica para o diagnóstico e tratamento de distúrbios abdominais e pélvicos, incluindo os órgãos reprodutivos femininos.
Continue a leitura e conheça melhor o funcionamento e indicações da técnica.
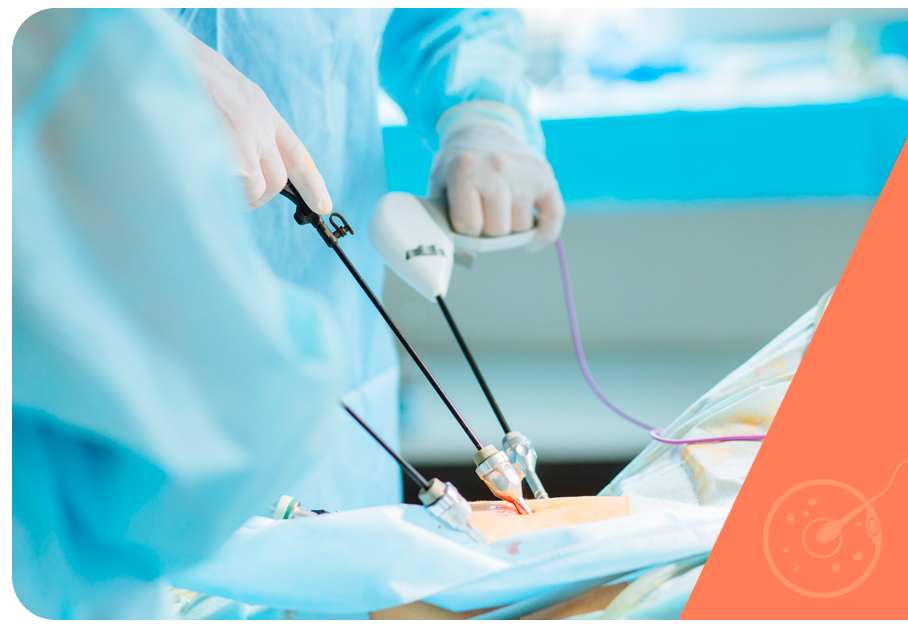
A videolaparoscopia é uma técnica minimamente invasiva que fornece uma vista panorâmica e ampliada dos órgãos abdominais ou pélvicos e permite o tratamento no momento do diagnóstico. A prática é conhecida pela medicina como see and treat ou ‘ver e tratar’.
Utiliza o laparoscópio, um dispositivo longo e delgado com uma câmera acoplada, inserido pelo abdômen a partir de pequena incisão com cerca de 1 cm. Dessa forma, possibilita a visualização da cavidade abdominal e órgãos reprodutores (útero, trompas e ovários) pelo especialista em tempo real.
Se o problema precisar ser corrigido, são feitas outras pequenas incisões para inserção de instrumentos cirúrgicos em miniatura, como tesouras e pinças.
Praticamente todas a cirurgias ginecológicas e urológicas podem ser realizadas por videolaparoscopia.
A técnica também pode ser utilizada em outros tipos de cirurgias, como a bariátrica, remoção de órgãos inflamados, incluindo vesícula, baço ou apêndice, para o tratamento de hérnias do abdome, remoção de tumores ou pólipos do cólon ou operações nas articulações (artroscopias), principalmente no joelho, mudando apenas a área na qual será introduzida a câmera.
Por ser minimamente invasiva provoca menor trauma cirúrgico, com cicatrizes praticamente invisíveis, menos sangramento intraoperatório, menor dor pós-operatória, além de a recuperação pós-cirúrgica ser mais rápida e permitir o retorno às atividades mais cedo.
Da mesma forma que possui baixas taxas de infecções e a ocorrência de aderências pós-operatórias.
Saiba quando a videolaparoscopia é indicada como ela pode auxiliar a reprodução assistida
A videolaparoscopia pode investigar a causa de dor pélvica crônica, infertilidade ou presença de massas. Na reprodução assistida, a cirurgia é destinada a melhorar a fertilidade e pode incluir intervenções no útero, ovários e tubas uterinas visando, por exemplo, liberar aderências nas trompas para viabilizar uma gravidez espontânea sem precisar de FIV (fertilização in vitro) ou até mesmo indicá-la (FIV), se confirmar que a função tubária está muito prejudicada.
Nas mulheres, a videolaparoscopia diagnóstica é realizada principalmente para identificar a causa de dor na região pélvica/ abdominal e ou infertilidade, na maioria das vezes, quando outros métodos não conseguem diagnosticar a causa desses sintomas.
Além disso, é o método padrão ouro para o diagnóstico e tratamento de endometriose. No entanto, a técnica também é importante para o tratamento de miomas uterinos, DIPA, gravidez ectópica, por exemplo, da mesma forma que pode ser utilizada para a remoção de órgãos como o útero.
Veja as principais indicações cirúrgicas da técnica, quando há problemas de fertilidade:
Outras indicações da videolaparoscopia para a saúde feminina:
O período de recuperação após a videolaparoscopia varia de acordo com o objetivo do procedimento. Quando é diagnóstico a mulher normalmente é liberada em até 12 horas após o procedimento, enquanto a cirúrgica pode ser necessário internação de 24 horas. O período de recuperação pode variar entre 7 e 14 dias e a atividades física, inclusive a relação sexual, devem ser evitadas na primeira semana.
Para entender melhor o funcionamento da videolaparoscopia, leia o nosso texto completo sobre o assunto.
MaisDurante a ejaculação, o sêmen é produzido a partir de uma suspensão concentrada de espermatozoides, armazenados nos dois epidídimos, misturados com e diluídos por secreções líquidas dos órgãos sexuais acessórios. Assim, seu objetivo é abrigar e transportar os gametas masculinos até as tubas uterinas para […]
Durante a ejaculação, o sêmen é produzido a partir de uma suspensão concentrada de espermatozoides, armazenados nos dois epidídimos, misturados com e diluídos por secreções líquidas dos órgãos sexuais acessórios. Assim, seu objetivo é abrigar e transportar os gametas masculinos até as tubas uterinas para que a fecundação ocorra.
A produção de espermatozoides acontece nos túbulos seminíferos, estruturas localizadas nos testículos e, posteriormente, armazenados e nutridos em outros dutos, os epidídimos, até se tornarem maduros para serem transportados e ejaculados.
O sêmen se forma nesse percurso, a partir da incorporação dos espermatozoides ao fluído seminal produzido pelas vesículas seminais e próstata. É cremoso, espumoso e esbranquiçado.
Quer saber o que é azoospermia? Continue a leitura.
A azoospermia é uma condição em que os espermatozoides não estão presentes no sêmen ejaculado. Diferentes fatores podem provocar a ausência de espermatozoides no sêmen, por isso a azoospermia é classificada como obstrutiva e não obstrutiva.
A obstrutiva é o tipo mais comum, caracterizada por um bloqueio que impede o transporte. Pode ocorrer nos epidídimos, dutos deferentes (que os transportam) ou ejaculatórios.
Já a não obstrutiva tem como característica a diminuição ou interrupção da produção de espermatozoides pelos testículos.
Veja abaixo as causas de azoospermia obstrutiva e azoospermia não obstrutiva:
As obstruções que impedem o transporte dos gametas masculinos geralmente são consequência de inflamações como epididimite, do epidídimo e orquite, dos testículos, frequentemente causadas por infecções sexualmente transmissíveis (IST), entre elas a clamídia e a gonorreia.
Os processos inflamatórios podem levar à formação de aderências, provocando, assim, as obstruções. No entanto, também podem resultar de tumores, cistos ou da ejaculação retrógada, quando o sêmen flui para bexiga em vez de sair pela uretra durante o orgasmo. Este tipo também é conhecido como azoospermia pós-testicular.
A azoospermia não obstrutiva é subdividida em pré-testicular e testicular. As causas de alterações na produção de espermatozoides, variam de acordo com cada subtipo.
Também são considerados fatores de risco para alterações na produção de espermatozoides, hábitos como alcoolismo, tabagismo, superexposição ao calor e a toxinas, quimioterapia ou radioterapia, obesidade ou mesmo alguns transtornos emocionais, incluindo ansiedade e depressão.
Homens com azoospermia não apresentam nenhum tipo de sintoma na maioria das vezes. Normalmente é percebida quando há dificuldade para engravidar a parceira. Se houver suspeitas, o especialista solicitará diferentes exames. Além de confirmar o problema, eles vão indicar o tipo que o causou.
O espermograma, exame padrão para avaliação da fertilidade masculina, é o primeiro solicitado. Além de confirmar a ausência de espermatozoides nas amostras de sêmen analisadas, aponta, ainda, possíveis anormalidades no líquido seminal.
Após a confirmação, são solicitados exames de sangue, que indicam a possibilidade de inflamações e a bactéria causadora, testes hormonais, para avaliar os níveis dos hormônios sexuais masculinos e, exames de imagem, como a ultrassonografia dos testículos com doppler e a ressonância magnética (RM), que verificam a presença de bloqueios.
Os resultados são importantes para definir a abordagem terapêutica mais adequada para cada paciente. Ainda que possa ter cura em muitos casos, quando o diagnóstico é realizado precocemente as chances são maiores.
A azoospermia está entre as causas mais comuns de infertilidade masculina. Nos casos em que o tratamento farmacológico ou cirúrgico não proporciona a restauração da fertilidade, a fertilização in vitro com injeção intracitoplasmática de espermatozoides (FIV com ICSI) é o tratamento indicado para possibilitar que esse homem tenha filhos.
Na FIV com ICSI, é possível recuperar os espermatozoides do epidídimo ou dos testículos com a utilização de diferentes abordagens cirúrgicas:
TESE, sigla em inglês para testicular sperm extraction, e Micro-TESE, ou microdissection testicular sperm extraction, são os métodos utilizados quando a azoospermia é não obstrutiva. Eles possibilitam a recuperação dos espermatozoides diretamente dos testículos.
Quando a azoospermia é obstrutiva, os espermatozoides são recuperados dos epidídimos. Os métodos utilizados são PESA (percutaneous epididymal sperm aspiration) e MESA (microsurgical epididymal sperm aspiration).
Desde a década de 1990 a azoospermia, assim como outros fatores graves de infertilidade masculina, pode ser tratada pela FIV com ICSI (injeção intracitoplasmática de espermatozoides), que utiliza diferentes métodos cirúrgicos para recuperação dos espermatozoides.
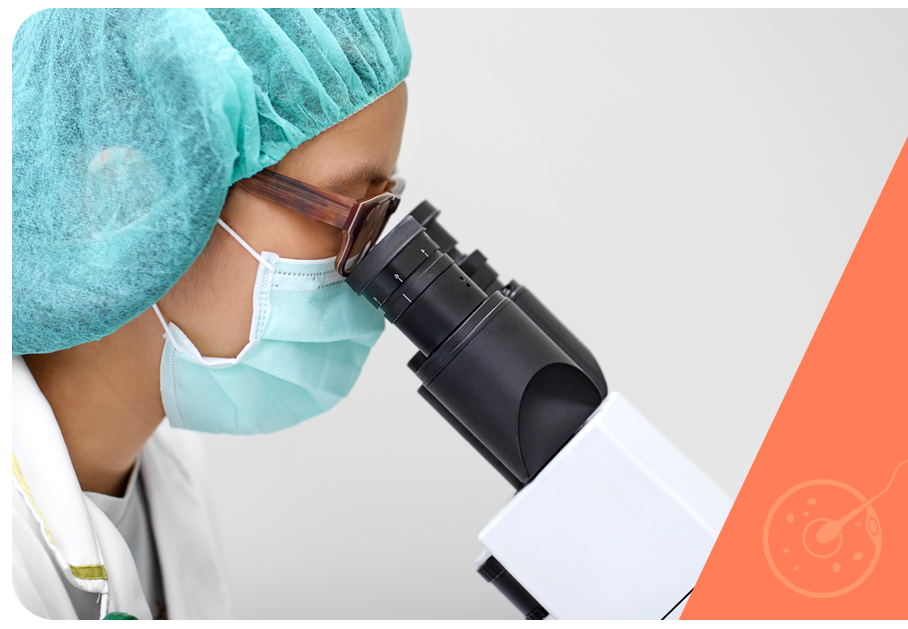
Depois de serem coletados, posteriormente os espermatozoides são avaliados individualmente por um microscópio de alta potência e injetados diretamente no óvulo pelo micromanipulador de gametas, um aparelho de alta precisão.
Os percentuais de sucesso da FIV com ICSI são bastante expressivos: de aproximadamente 40% a 60%.
Saiba mais detalhes sobre a azoospermia em nosso conteúdo elaborado especificamente para isso.
MaisA quantidade de folículos ovarianos (que envolvem os óvulos individualmente) é chamada reserva ovariana e diminui de forma natural durante toda a vida, inclusive antes da puberdade (...) a perda da reserva ovariana não pode ser evitada, porém sua taxa pode ser estimada por exames, que ajudam na avaliação da fertilidade da mulher.
Quando um casal planeja ter filhos, muitos são os fatores que devem ser levados em consideração nessa tomada de decisão, sendo a idade da mulher um dos mais importantes, uma vez que com o tempo sua fertilidade diminui.
A partir dos 35 anos de idade, os gametas femininos (óvulos) passam a perder qualidade e diminuir em quantidade de forma mais intensa, processo que acontece de forma progressiva com o avanço da idade.
A quantidade de folículos ovarianos é chamada reserva ovariana e diminui de forma natural durante toda a vida, inclusive antes da primeira menstruação.
Mesmo com o uso de anticoncepcionais que inibem a ovulação, a cada ciclo menstrual são perdidos cerca de mil óvulos. A perda da reserva ovariana não pode ser evitada. No entanto, podemos avaliá-la com exames, que ajudam na avaliação da fertilidade da mulher.
Quer saber como essa avaliação é feita? Acompanhe o texto!
Reserva ovariana é a quantidade de folículos disponíveis para amadurecimento e ovulação, chamados folículos antrais. A quantidade de gametas femininos disponível para toda a vida da mulher está presente já no período intrauterino e não aumenta durante a vida.
Na vida intrauterina, por volta da 20ª semana de gestação, a reserva ovariana conta com cerca de 7.000.000 de oócitos, que ao nascimento já são cerca de 2.000.000 e na puberdade chegam a 200.000 a 300.000. Na menopausa, a reserva ovariana acaba, impossibilitando a gestação.
A diminuição da reserva ovariana é gradativa a partir da puberdade, acentuando-se aos 35 anos e ainda mais depois dos 40 anos.

A avaliação da fertilidade feminina, assim como da masculina, é individualizada. Inicia-se na anamnese com avaliação do histórico familiar e individual da mulher ou do casal, em que são analisados fatores como qualidade de vida, idade, gestações ou partos precedentes, bem como a possibilidade de distúrbios que possam trazer complicações para a gestação. Dependendo desse histórico inicial, a avaliação é encaminhada.
O principal objetivo dessa investigação da infertilidade é indicar a técnica de reprodução assistida mais adequada para cada caso, sendo a avaliação da reserva ovariana uma etapa importante.
Existem dois procedimentos para estimar a reserva ovariana de uma mulher: dosagem das concentrações séricas dos hormônios FSH (folículo-estimulante) associado à dosagem do estradiol e HAM (hormônio antimülleriano) e ultrassom transvaginal para contagem de folículos antrais (que têm o potencial de amadurecer e ovular).
Espera-se que mulheres com 35 anos ou mais já tenham uma reserva ovariana reduzida, enquanto as mais jovens apresentem reserva preservada.
Os resultados não são uma sentença. Eles se somam aos resultados de outros exames para que seja tomada a melhor decisão. Ainda existem muitos estudos relacionados aos exames que avaliam a reserva ovariana.
Resultados que mostram altas concentrações de FSH e baixas concentrações de HAM podem indicar que está havendo uma perda da reserva ovariana, assim como quando o resultado da contagem de folículos é baixa.
Os exames de reserva ovariana sugerem FOP (falência prematura ovariana) quando há um comprometimento severo da reserva antes dos 40 anos, mas seus resultados também são úteis na avaliação do potencial de fertilidade de mulheres mais velhas que desejam engravidar.
Como fica simples concluir, a diminuição da reserva ovariana é um indicador para urgência reprodutiva, dando o diagnóstico de diminuição da fertilidade feminina.
Quando uma baixa reserva ovariana é diagnosticada, as técnicas de reprodução assistida podem ser indicadas para que o casal possa ter filhos. Pode ser indicada a RSP (reprodução sexual assistida) e/ou IIU (inseminação intrauterina), se a mulher tiver até 35 anos com as tubas uterinas preservadas e parceiro com espermograma normal, ou a fertilização in vitro (FIV), principalmente quando há outros fatores associados.
Em ambas as técnicas é feita a estimulação ovariana, tratamento que estimula o crescimento de um número maior de folículos e a ovulação. Dependendo do comprometimento da reserva ovariana, a resposta à estimulação não é satisfatória, por isso é importante estudar cada caso individualmente.
Na RSP e/ou IIU, o objetivo é estimular o crescimento de 1 a 3 folículos. Um número maior de folículos aumenta o risco de gestação gemelar, portanto o tratamento é cancelado nesse caso. Depois da estimulação, orientamos o casal sobre qual é o melhor momento para ter as relações sexuais ou fazer a IIU.
Na FIV, a estimulação ovariana é feita de outra forma. Um número maior de folículos é estimulado a amadurecer, uma vez que não há risco de gestação gemelar nessa etapa. Quando, durante o controle ultrassonográfico do desenvolvimento dos folículos, identificamos que eles estão maduros, induzimos a ovulação com medicamentos hormonais.
Pouco antes da ovulação, o líquido folicular é aspirado e enviado ao laboratório, que separa os óvulos para fecundação. Ao mesmo tempo é feita a coleta e o preparo do sêmen. Óvulos e espermatozoides são colocados em uma placa de cultivo e são fecundados. Os espermatozoides são injetados dentro dos óvulos. As chances de fecundação são muito altas.
Os embriões formados são cultivados em laboratório por alguns dias. A etapa final é a transferência dos embriões ao útero. Alguns dias depois, o casal já pode fazer o tão esperado teste de gravidez. Cerca de 20% a 60% dos casos são bem-sucedidos.
Essas taxas de sucesso variam muito, a depender, principalmente, de se obter bons embriões para transferir ao útero, sendo sensivelmente afetadas quando a reserva ovariana está comprometida. Quando a notícia não é positiva na primeira vez, o casal pode tentar novamente quantas vezes forem necessárias.
Toque aqui e saiba mais sobre as formas de se diagnosticar a infertilidade!
Mais
