A escolha do melhor momento para a transferência embrionária deve ser feita de forma individualizada, de acordo com as especificidades de cada caso, especialmente relacionadas à qualidade e ao número de embriões viáveis, obtidos após a fecundação.
A FIV (fertilização in vitro) é, atualmente, a técnica de reprodução assistida mais abrangente e com as melhores taxas de gestação – indicada para a maior parte dos casos de infertilidade, para preservação social e oncológica da fertilidade e para o atendimento de casais homoafetivos que desejam ter filhos.
A primeira vez que um tratamento com reprodução assistida utilizou a fertilização em ambiente laboratorial, a partir de gametas coletados e resultando em gestação, aconteceu na Inglaterra, em 1979, dando início a história da FIV.
A partir de então, a técnica vem se desenvolvendo e incorporando tecnologias complementares, como o preparo seminal, o PGT (teste genético pré-implantacional), hatching assistido, entre outros procedimentos, que aumentaram sua acurácia e por isso o sucesso da técnica.
Atualmente é possível, inclusive, escolher qual o melhor momento para realizar a transferência embrionária, com base no comportamento do embrião durante o cultivo embrionário, diminuindo as chances de perda gestacional e falha em um ciclo de tratamento com FIV.
Este texto mostra quais fatores estão envolvidos na decisão pelo melhor momento para realizar a transferência embrionária. Nos acompanhe na leitura a seguir e entenda melhor essa importante etapa da FIV.
A maior parte das técnicas de reprodução assistida é realizada em etapas sequenciais e interdependentes, e no caso da FIV são cinco: estimulação ovariana, coleta de gametas, fecundação, cultivo embrionário e transferência dos embriões.
A etapa de estimulação ovariana tem início logo após o primeiro dia do ciclo menstrual, e é realizada com administração de doses diárias das gonadotrofinas FSH (hormônio folículo-estimulante) associado ao LH (hormônio luteinizante) desde o início do tratamento ou no meio deste, a depender do contexto da paciente.
O objetivo desta etapa é potencializar o ciclo reprodutivo, provocando o amadurecimento de 10 a 15 folículos ovarianos. Este processo deve ser monitorado por ultrassonografia transvaginal, que indica o melhor momento para dar início a etapa seguinte.
Quando os folículos ovarianos atingem o auge do processo de amadurecimento, a coleta de gametas, masculinos e femininos, deve ser realizada.
A coleta dos folículos só pode ser feita por aspiração folicular, uma técnica de punção realizada diretamente nos ovários. Já a coleta de espermatozoides pode ser feita por masturbação ou, nos casos em que a infertilidade é causada por azoospermia obstrutiva, os espermatozoides também podem ser obtidos por punção, diretamente nos túbulos seminíferos ou nos epidídimos.
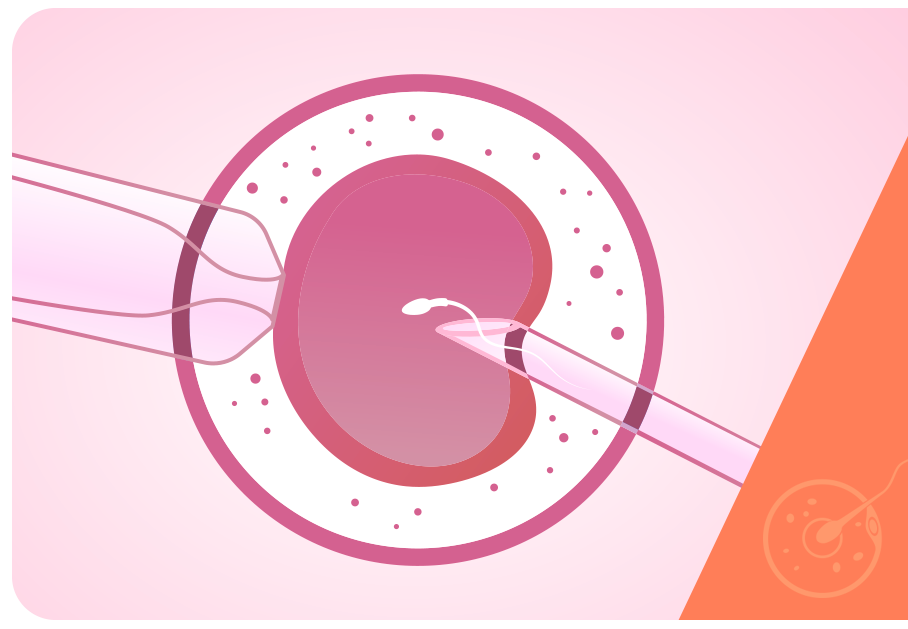
A partir da coleta e seleção dos gametas, a fecundação é realizada com a união das células em ambiente laboratorial. A ICSI (injeção intracitoplasmática de espermatozoide) é uma técnica complementar bastante utilizada hoje, e que possibilita a seleção de um único espermatozoide e sua introdução no interior do ovócito, com auxílio de uma agulha especial.
Os embriões obtidos na fecundação são então cultivados, por um período que varia entre 3 e 5 dias, dependendo dos objetivos do tratamento com FIV (congelamento de embriões ou transferência de embriões frescos) e da qualidade dos embriões.
Durante o cultivo embrionário é possível observar alterações nos processos de divisão celular, típicos dessa fase embrionária, podendo também realizar o PGT, uma técnica complementar que rastreia as possibilidades de os embriões serem portadores de doenças genéticas e hereditárias.
A transferência embrionária é a última etapa da FIV e deve ser realizada após o cultivo embrionário.
A determinação do melhor momento para realizar a transferência embrionária depende do comportamento que o embrião apresenta durante seu desenvolvimento, observado no cultivo embrionário.
Até o terceiro dia de cultivo, ou D3, o embrião passa por clivagens suficientes para uma primeira avaliação de suas possibilidades de implantação. A partir do quarto dia, já inicia a compactação das células, formação da mórula para que no quinto ou sexto dia (D5/D6) esteja em estágio de blastocisto.
Ainda que as melhores taxas de implantação embrionária se refiram a procedimentos realizados em D5, a transferência em D3 é possível e pode ser indicada em situações específicas.
A transferência embrionária é um procedimento simples, realizado no bloco cirúrgico da clínica, sem a necessidade de anestesia.
A única preparação para transferência embrionária é que a mulher se apresente com a bexiga cheia, que facilita a visualização da cavidade uterina pelo ultrassom que acompanha o procedimento.
A mulher deve deitar-se em posição ginecológica, para que seja introduzido via canal vaginal o cateter contendo os embriões. Na outra extremidade desse cateter encontra-se uma espécie de êmbolo que empurra os embriões para o interior da cavidade uterina, onde devem ser implantados na superfície do endométrio.
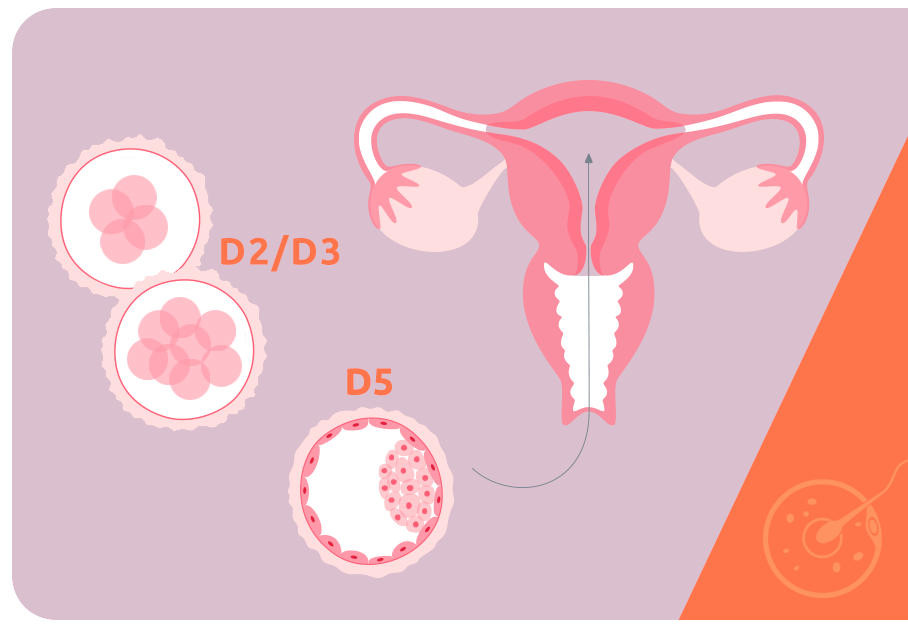
A escolha do melhor momento para a transferência embrionária deve ser feita de forma individualizada, de acordo com as especificidades de cada caso, especialmente relacionadas à qualidade e ao número de embriões viáveis, obtidos após a fecundação.
Nos tratamentos com a FIV em que o cultivo embrionário mostra poucos embriões já na fase de D3, o mais aconselhável é realizar a transferência embrionária neste momento, para que haja menos manipulação dos embriões.
Nestes casos, a implantação embrionária pode ser favorecida pelo hatching assistido, uma tecnologia complementar da FIV, em que a zona pelúcida embrionária, que ainda está conservada em D3, é rompida artificialmente pelo embriologista, imediatamente antes da transferência embrionária.
Além dos fatos observados durante a etapa de cultivo embrionário, alguns fatores devem ser considerados para tomar a decisão a respeito do melhor momento para realizar a transferência embrionária.
Um dos principais fatores é a idade da mulher que está realizando o tratamento com a FIV. Sabe-se que mulheres com mais de 35 anos podem apresentar alterações hormonais, especialmente relacionadas aos estrogênios, que interferem na receptividade endometrial.
Nestes casos, a mulher deve passar pela preparação endometrial, feita com administração de medicamentos hormonais à base de estrogênio e progesterona, e a transferência embrionária deve ser realizada no momento indicado pelo monitoramento ultrassonográfico desta etapa, a partir de D3.
Quer saber mais sobre a FIV? Acesse nosso conteúdo.
MaisNas técnicas de reprodução assistida em que o preparo seminal é possível, este procedimento pode ser feito a partir de tecnologias de seleção espermática, que usam diferentes métodos para se adequar às necessidades impostas pela doença.
A fertilidade masculina está diretamente ligada a qualidade do sêmen, líquido expelido durante a ejaculação e que contém os espermatozoides e os líquidos produzidos pelas glândulas anexas: próstata, vesícula seminal e glândula bulbouretral.
O plasma seminal, como é chamado o conjunto de líquidos glandulares, tem como principais funções nutrir os espermatozoides e proporcionar um meio alcalino, para que estes espermatozoides sejam conduzidos, no interior do sistema reprodutivo feminino, sem que a acidez natural do canal vaginal danifique essas células.
Assim, a maior parte das alterações na composição do sêmen e nas estruturas envolvidas no trajeto percorrido pelo esperma durante a ejaculação, podem se refletir em prejuízos para a função reprodutiva masculina.
A maior parte dos casos de infertilidade masculina pode ser solucionada pelas técnicas de reprodução assistida, desenvolvidas e disponibilizadas pela medicina reprodutiva atualmente, com destaque para a FIV (fertilização in vitro) e a IA (inseminação artificial).
O preparo seminal é um conjunto de procedimentos, realizados com o objetivo de selecionar os espermatozoides mais viáveis para reprodução assistida. Essa tecnologia complementar aumentou consideravelmente as taxas de gestação para FIV e IA, melhorando a abrangência dessas técnicas para casos mais complexos de infertilidade masculina.
Acompanhe a leitura do texto a seguir e entenda o que é o preparo seminal, como ele é utilizado na reprodução assistida e em quais situações deve ser indicado.
O preparo seminal é um procedimento realizado na FIV e na IA, com o objetivo de melhorar a qualidade da amostra de sêmen e, com isso, otimizar as chances de fecundação – especialmente nos casos em que a infertilidade masculina se deve a alterações espermáticas.
As principais alterações seminais, que levam à infertilidade, incidem na qualidade ou na concentração dos espermatozoides no líquido ejaculado, e podem ser identificadas pelo espermograma, um exame fundamental para a indicação do preparo seminal.
Este exame detecta se a amostra de sêmen contém poucos ou nenhum espermatozoide (oligozoospermia e azoospermia, respectivamente), se existem problemas de motilidade (astenozoospermia) ou alterações morfológicas (teratozoospermia), que trazem dificuldades para a fecundação.
Nas técnicas de reprodução assistida em que o preparo seminal é possível, este procedimento pode ser feito a partir de tecnologias de seleção espermática, que usam diferentes métodos para se adequar às necessidades impostas pela doença responsável pela infertilidade masculina.
O preparo seminal pode ser realizado a partir de diferentes técnicas que compartilham o mesmo objetivo de selecionar os melhores gametas masculinos para a fecundação.
Após a coleta, geralmente por masturbação, a amostra seminal é avaliada para definir qual técnica será mais adequada para o preparo.
Entre as técnicas de preparo seminal mais utilizadas, destacamos a lavagem seminal (sperm wash), a migração ascendente (swim-up) e o gradiente descontínuo de densidade.
Dependendo das alterações seminais presentes na amostra, pode ser necessária a associação de diferentes técnicas de preparo seminal.
A lavagem seminal, ou sperm wash, é a técnica mais simples de preparo seminal e consiste em submeter a amostra de sêmen, depositada no interior de um tubo de ensaio e sem um meio de cultura específico, a uma intensa força centrífuga, capaz de separar o plasma seminal dos espermatozoides.
Essa técnica é indicada principalmente para casos em que a amostra de sêmen apresenta uma baixa concentração de espermatozoides.
Na migração ascendente, ou swim-up, a amostra de sêmen é depositada no fundo de um tubo de ensaio preenchido por um meio de cultura cuja densidade é diferente da encontrada na amostra seminal, com o objetivo de fazer com que os espermatozoides mais viáveis se desprendam do fundo do tubo e nadem em direção à superfície.
O material sobrenadante é então coletado por uma pipeta especial, para ser utilizado.
O swim-up é indicado para os casos em que amostra seminal encontra-se normal em concentração e motilidade.
No gradiente descontínuo de densidade, o tubo de ensaio deve conter meios de cultura com diferentes densidades, e a amostra de sêmen é depositada na superfície do tubo, e então submetido a uma força centrífuga.
A diversidade de densidades obriga os espermatozoides a nadar com intensidades diferentes, a partir do momento em que a centrífuga é ativada.
Este é um método mais rápido e mais apto a selecionar espermatozoides com melhor morfologia e motilidade, mas que pode apresentar uma concentração espermática mais baixa.
O principal benefício, decorrente do desenvolvimento do preparo seminal, é um aumento no nível de seleção das células reprodutivas masculinas, que favorece a realização de fecundações mais bem-sucedidas, tanto para IA, quanto para FIV.
Foi a partir do preparo seminal, também, que outras técnicas complementares passaram a ser possíveis, como é o caso da ICSI (injeção intracitoplasmática de espermatozoide), cada vez mais utilizada para realizar a fecundação na FIV.
Na ICSI, um único espermatozoide é selecionado para fecundar o óvulo. O preparo seminal é a forma pela qual essa unidade de espermatozoide pode ser selecionada.
Para saber mais acesse o link.
MaisNem sempre, porém, os homens e mulheres que recebem o diagnóstico oncológico são informados adequadamente sobre as possibilidades de preservação oncológica da fertilidade.
Ainda hoje, receber a notícia de um diagnóstico para o câncer pode provocar fortes emoções e preocupações a respeito das possibilidades de sobrevivência, embora a taxa de sobrevivência venha aumentando muito, devido aos avanços nos tratamentos desenvolvidos durante as últimas décadas.
A radioterapia e a quimioterapia são os principais tratamentos oncológicos disponíveis atualmente. Estes tratamentos, ainda que bastante bem-sucedidos, podem ser agressivos especialmente às células reprodutivas (óvulos e espermatozoides), mesmo quando o câncer não afeta qualquer estrutura do sistema reprodutivo de homens e mulheres.
A preservação oncológica da fertilidade é, por isso, um direito da pessoa em tratamento para os diversos tipos de câncer, já que possibilita o congelamento das células reprodutivas e embriões antes do início do tratamento, aumentando as chances de que a gestação aconteça, após o final do tratamento.
A FIV (fertilização in vitro) e a IA (inseminação artificial) são as duas técnicas de reprodução assistida utilizadas para a preservação oncológica da fertilidade.
Embora a FIV apresente maiores taxas de sucesso, nos casos em que é o homem quem procura essa ferramenta – e sua companheira não apresenta qualquer fator de infertilidade –, a IA pode ser realizada e apresenta uma melhor relação custo-benefício.
Esse texto mostra como a preservação oncológica da fertilidade abre possibilidades para que homens e mulheres, em tratamento para o câncer, possam continuar caminhando em busca de realizar seus planejamentos familiares.
O câncer é considerado um problema de saúde pública global e configura entre os quatro principais motivos da morte de pessoas com mais de 70 anos de idade.
Esse aumento da incidência do câncer, nas últimas décadas, reflete um aumento na expectativa de vida geral da população, que hoje envelhece até mais tarde e por isso é mais diagnosticada; mas também é decorrente das mudanças no estilo de vida da sociedade contemporânea, mais acelerada e estressante.
As origens etiológicas do câncer são consideradas multifatoriais, já que apesar de existir uma forte predisposição genética (quando existem outros casos de câncer na família), fatores ambientais, como a exposição à radiação, uso de substâncias tóxicas – como o tabaco – e um estilo de vida muito estressante, também participam dos gatilhos que disparam câncer.
Nesta doença, algumas células passam a apresentar um comportamento imprevisível, resultante de alterações genéticas hereditárias ou de mutações causadas por estresse oxidativo.
Essas células passam a não desempenhar suas funções corretamente e multiplicar-se de forma desordenada. As células resultantes dessas multiplicações são igualmente imprevisíveis e, após um período de tempo – proporcional à agressividade do câncer – os tecidos e órgãos afetados podem ter suas funções severamente comprometidas.
A radioterapia e a quimioterapia são os tratamentos oncológicos disponíveis para os diversos tipos de câncer atualmente, e consistem em metodologias que buscam destruir as células doentes, sem que o tecido precise ser retirado, e evitando a continuação do processo de multiplicação.
A radioterapia utiliza a emissão de radiação controlada e direcionada à área onde localizam-se as células doentes, enquanto a quimioterapia é realizada por via medicamentosa, através de substâncias que rastreiam as células anômalas e destroem-nas.
Como as doses de radiação e medicamentos dependem do tamanho e da localização do tumor – e na maior parte das vezes precisam ser mais agressivos para buscar melhores taxas de sobrevivência –, os tratamentos podem afetar células que não estão doentes, como os gametas, provocando sua destruição.
A destruição dos gametas de homens e mulheres é grave, havendo uma queda importante da sua função reprodutiva. Por isso, a preservação oncológica da fertilidade é uma forma de abrir espaço para a possibilidade de ter filhos após o tratamento.
Nem sempre os homens e mulheres que recebem o diagnóstico oncológico são informados adequadamente sobre as possibilidades de preservação oncológica da fertilidade.
Por isso, é importante que essa possibilidade seja apresentada da forma mais precoce possível, para que os pacientes oncológicos possam ter a perspectiva de que ao menos seu planejamento familiar não precise ser obrigatoriamente prejudicado pela doença.

A preservação oncológica da fertilidade é feita a partir do congelamento de óvulos, espermatozoides e embriões, que podem ser preservados por tempo indeterminado, e utilizados após o tratamento oncológico.
Para o congelamento de espermatozoides, uma amostra do sêmen deve ser obtida por masturbação, numa clínica específica e imediatamente encaminhada para o processo de criopreservação.
No caso dos óvulos, a mulher deve realizar a estimulação ovariana, com administração de gonadotrofinas exógenas para indução da ovulação, e a coleta é realizada por aspiração folicular, com auxílio de uma agulha de punção.
É importante lembrar que, para o congelamento de embriões, é preciso realizar a fecundação antes do processo de vitrificação, em laboratório. Os embriões são normalmente preservados após o terceiro dia de cultivo embrionário, podendo permanecer preservados por tempo indeterminado.
Após o fim do tratamento e a constatação de cura, esses materiais biológicos podem ser descongelados e os processos envolvidos nas reprodução assistida podem ser retomados, com o objetivo de conseguir a gestação.
Para saber mais acesse o link.
MaisNo caso da histeroscopia ambulatorial, a tecnologia da endoscopia é utilizada quase que exclusivamente como exame, permitindo intervenções somente para a ressecção de pequenas aderências uterinas e a coleta de material biológico destinado a biópsia.
O grande benefício que a criação dos exames de imagem trouxe para a medicina, foi a possibilidade de observar o interior do corpo humano em tempo real – e, atualmente, inclusive ao vivo e em formato de vídeo –, sem a necessidade de qualquer tipo de procedimento cirúrgico.
Atualmente, o desenvolvimento dos aparelhos que realizam os exames de imagem tem seguido a tendência de, cada vez mais, possibilitar a estratégia “see and treat” – literalmente “ver e tratar” -, em que o exame de imagem que confirma o diagnóstico e seu respectivo tratamento, sejam feitos na mesma ocasião.
A histeroscopia é um exemplo de exame de imagem que permite realizar simultaneamente o diagnóstico final – histeroscopia ambulatorial – e o tratamento – histeroscopia cirúrgica – para doenças como pólipos endometriais, sinequias e alguns tipos de miomas uterinos.
A histeroscopia ambulatorial é a forma mais simples de histeroscopia, e este texto aborda o que é e como este exame é realizado, nos acompanhe na leitura a seguir!
A histeroscopia é uma modalidade da endoscopia, neste caso, realizada através da introdução do endoscópio no canal vaginal e uterino, para a observação dessas estruturas.
No caso da histeroscopia ambulatorial, a tecnologia da endoscopia é utilizada quase que exclusivamente como exame, permitindo intervenções somente para a ressecção de pequenas aderências uterinas e a coleta de material biológico destinado a biópsia.
A estratégia “see and treat”, entretanto, é mais bem aplicada na histeroscopia cirúrgica, que utiliza a mesma tecnologia que a histeroscopia ambulatorial, para obtenção de imagens, porém é realizada em ambiente hospitalar, com raquianestesia ou sedação, e permitindo a intervenção no quadro identificado.

O endoscópio utilizado nas duas modalidades de histeroscopia é um pequeno aparelho cilíndrico, dotado de uma fonte de luz e uma câmera, com capacidade para obter imagens estáticas (fotos) ou em tempo real (vídeo), do interior do aparelho reprodutivo feminino.
Como preparação para a histeroscopia diagnóstica, recomenda-se que a mulher evite relações sexuais e o uso de cremes vaginais nas 72 horas que antecedem o procedimento, e pode ser aconselhável o uso de analgésicos abdominais, administrados por via oral, aproximadamente 40 minutos antes do exame, para diminuir a sensação de incômodo e possíveis cólicas.
Diferente da modalidade cirúrgica, a histeroscopia ambulatorial é um exame que pode ser feito fora do ambiente hospitalar, incluindo ambulatórios e clínicas, e não requer o uso de raquianestesia ou sedação.
Este procedimento é realizado com a mulher em posição ginecológica, para que o endoscópio seja introduzido no canal vaginal. As imagens obtidas são transmitidas para o monitor, e podem ser assistidas pela equipe médica e pela paciente que está se submetendo ao exame.
A histeroscopia ambulatorial é um exame rápido e que não demanda qualquer tipo de repouso posterior, outra diferença para a histeroscopia cirúrgica, em que a mulher normalmente necessita de repouso pós-operatório, e cuja duração depende dos procedimentos realizados no interior do aparelho reprodutivo.
Por tratar-se de um exame capaz de obter imagens detalhadas do canal vaginal, colo do útero, cavidade uterina e parte das tubas uterinas, as principais indicações para histeroscopia ambulatorial buscam concluir diagnósticos de doenças como miomas uterinos, pólipos endometriais, adenomiose e malformações uterinas.
A histeroscopia ambulatorial também é um exame bastante solicitado durante a investigação das causas da infertilidade feminina, especialmente quando a mulher apresenta o fator uterino como causa de infertilidade, porém é assintomática para outros sinais, já que o exame permite uma observação bastante detalhada do interior da cavidade uterina.
Mesmo para os casos em que a mulher está em tratamento com técnicas de reprodução assistida a histeroscopia ambulatorial ou diagnóstica pode ser importante de forma preventiva, para confirmar a integridade do endométrio, especialmente nos casos em que a mulher apresenta histórico de doenças uterinas precedentes.
Isso porque, independente da técnica de reprodução assistida escolhida, toda a gravidez acontece no interior da cavidade uterina, sendo fundamental que esta estrutura se apresente íntegra, diminuindo as chances de perdas gestacionais por dificuldades com a implantação embrionária, ou com a condução da gestação como um todo.
Quer mais detalhes sobre a histeroscopia ambulatorial? Acesse nosso link.
MaisA varicocele é atualmente considerada uma das principais causas de infertilidade masculina.
A infertilidade conjugal é um problema de saúde que afeta aproximadamente 15% de toda a população mundial. Estima-se que aproximadamente 40% dos casos, a infertilidade seja causada por problemas exclusivamente masculinos, fazendo da infertilidade masculina um assunto de profundo interesse para a medicina reprodutiva.
A infertilidade masculina pode ser causada por problemas genéticos ou adquiridos, que afetam a produção de espermatozoides (espermatogênese) ou causam obstruções no trajeto percorrido por essas células, durante a ejaculação.
É possível identificar a presença de alterações espermáticas pela análise do espermograma, e a partir dele solicitar exames complementares que possam apontar as causas dessas alterações espermáticas, como o ultrassom de bolsa escrotal, fundamental para o diagnóstico da varicocele.
A varicocele é atualmente considerada uma das principais causas de infertilidade masculina. As alterações decorrentes dessa doença, podem interferir na espermatogênese, levando a um quadro de azoospermia não obstrutiva, e se não tratada a tempo e de forma adequada, pode evoluir para infertilidade permanente.
Esse texto mostra como a varicocele está relacionada com danos à saúde reprodutiva masculina, e as atuais possibilidades de tratamento e reversão da infertilidade.
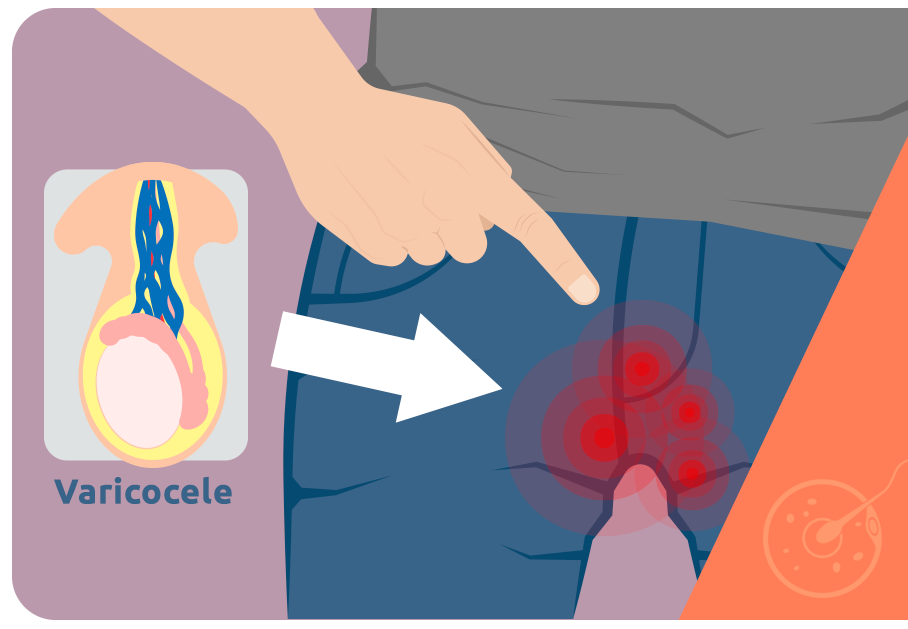
A varicocele é uma doença genética que afeta o plexo pampiniforme, responsável pela drenagem de sangue venoso da região dos testículos e da bolsa escrotal. As veias que irrigam essa região, nos casos de varicocele, contêm válvulas defeituosas, que não são capazes de manter o fluxo sanguíneo em uma única direção.
Isso faz com que o sangue fique estagnado, o que leva uma dilatação do plexo pampiniforme, e consequentemente a compressão do cordão espermático e o aumento na pressão na temperatura interna da bolsa escrotal.
Na maior parte das vezes, a varicocele é uma doença assintomática, porém quando manifesta sintomas, estes já podem ser observados a partir da puberdade.
Os principais sintomas da varicocele são a sensação de dor e peso nos testículos, causado pelo acúmulo de sangue, diminuição do volume testicular e infertilidade. Nos casos mais graves, é possível observar a dilatação da rede venosa a olho nu, pela presença de vasos arroxeados e visíveis na superfície da bolsa escrotal.
A infertilidade é apenas um dos sintomas possíveis da varicocele, embora essa doença seja considerada, atualmente, a principal causa de infertilidade masculina. O aumento da temperatura e da pressão testiculares interfere no processo de amadurecimento do espermatócito, a célula reprodutiva primordial que origina os espermatozoides.
Os prejuízos que a varicocele causa à espermatogênese podem resultar em quadros de azoospermia, ausência de espermatozoides no sêmen, ou teratozoospermia, uma grande quantidade de espermatozoides inviáveis por alterações morfológicas.
Aproximadamente 30% dos casos de infertilidade primária (quando o homem nunca teve filhos) são causados pela varicocele, mas se observarmos a proporção de homens com infertilidade secundária, esse número sobe para 80% dos casos.
Por isso, é importante lembrar que os efeitos da varicocele na função reprodutiva masculina têm caráter progressivo e, mesmo nos casos assintomáticos, a fertilidade pode estar sendo prejudicada de forma silenciosa.
Por ser predominantemente assintomática, muitas vezes o diagnóstico da varicocele só é feito em exames de rotina, para o homem que cuida com regularidade de sua saúde reprodutiva.
Quando esta doença é detectada, a escolha pelo melhor tratamento deve estar baseada na intensidade dos sintomas dolorosos e no desejo do homem de ter filhos.
A correção da varicocele é a única forma de tratar os defeitos valvulares provocados por essa doença genética. Ela é feita geralmente por sedação ou raquianestesia e o tempo de recuperação varia entre 10 a 15 dias após o procedimento cirúrgico. Durante esse período, o homem pode levar boa parte de sua vida cotidiana, embora tenha que evitar esforços físicos mais acentuados.
Apesar das boas taxas de sucesso da correção cirúrgica para varicocele, muitos profissionais ainda questionam a validade do procedimento, especialmente porque a varicocelectomia, como também é chamada a cirurgia de correção da varicocele, é invasiva e a melhora nos valores do espermograma são mais expressivas apenas nos casos sintomáticos e com grau de varicocele mais importante.
As técnicas de reprodução assistida são também indicadas como tratamento, para os casos de infertilidade por varicocele, principalmente a FIV (fertilização in vitro), quando a alteração no sêmen é de moderada a severa.
E nos casos de azoospermia, a coleta de espermatozoides pode ser feita por punção testicular ou epididimária. Quando a alteração no sêmen é leve, há a possibilidade de se recorrer à IA (inseminação artificial).
Entenda melhor o que é varicocele acompanhando nosso conteúdo.
MaisO tempo realmente é um fator preponderante para o sucesso da reversão da vasectomia, porém está mais relacionado a perda natural da fertilidade, que acontece com o passar do tempo, tanto para homens quanto para mulheres.
É comum que casais, normalmente já com filhos, procurem a vasectomia como método contraceptivo definitivo, inclusive de forma preferencial a laqueadura tubária, por ser uma cirurgia mais simples.
É possível que parte dos homens que realizam a vasectomia, se arrependam do procedimento, e voltem a manifestar o desejo de ter filhos. É importante lembrar que a vasectomia tem 99,99% de eficiência contraceptiva, mas é uma cirurgia que leva à esterilidade masculina definitiva, por isso é uma decisão que deve ser tomada de forma cautelosa.
A reversão da vasectomia é um procedimento possível, ainda que mais complicado e delicado do que a própria vasectomia. Para que a reversão seja indicada, alguns aspectos devem ser rigorosamente observados, especialmente relacionados ao tempo decorrido entre a vasectomia e a reversão, bem como a fertilidade da mulher com quem se deseja ter filhos.
Nesse sentido, é imprescindível realizar uma avaliação acurada da saúde reprodutiva do casal como um todo, para que a reversão da vasectomia possa ser indicada de forma adequada.
Nos casos em que a reversão é contraindicada, também é importante que o casal possa conhecer as técnicas de reprodução assistida mais adequada para sua situação específica.
Neste texto, mostraremos em que momento a reversão da vasectomia é indicada e, caso seja contraindicada, quais saídas a medicina reprodutiva pode oferecer para o casal que deseja ter filhos.
A vasectomia é uma cirurgia minimamente invasiva, que provoca a esterilidade definitiva dos homens.
O procedimento é realizado a partir de pequenos cortes na bolsa escrotal, para o acesso aos canais deferentes, localizados no cordão espermático e que conduzem o sêmen e os espermatozoides à uretra. O bloqueio dos canais deferentes pode ser feito com grampos cirúrgicos, cauterização ou sutura.
Todas as formas de obstrução dos canais deferentes são igualmente efetivas para a esterilização, embora a retirada dessas obstruções, realizada durante a reversão da vasectomia, apresente dificuldades variadas dependendo do tipo de bloqueio utilizado.
A cirurgia de reversão da vasectomia é relativamente mais complexa do que a própria vasectomia.
Nesse procedimento, é necessário encontrar o local em que os ductos deferentes foram bloqueados, com auxílio de um microscópio, para que os materiais utilizados para bloqueio possam ser retirados, como no caso dos grampos cirúrgicos e esses canais possam ser religados.
A reversão da vasectomia é, assim como a vasectomia, uma cirurgia pouco invasiva, realizada com uso de anestesia raquidiana. Após a cirurgia, o homem deve fazer repouso para guardar o retorno do efeito anestésico, no próprio hospital, podendo dar andamento às suas atividades cotidianas já no dia seguinte.
O sucesso da reversão depende de alguns fatores, como o tempo decorrido entre a vasectomia e a sua reversão, o tipo de técnica empregada na vasectomia e o funcionamento específico da cicatrização, que varia de caso a caso.
Além disso durante o procedimento é possível observar se a produção testicular de espermatozoides foi conservada e se existem gametas masculinos no líquido do ducto deferente, em sua porção mais testicular, mostrando que a espermatogênese não foi afetada.
Em teoria, é possível tentar a reversão da vasectomia em qualquer caso, porém alguns aspectos devem ser avaliados para tomar essa decisão, com o objetivo de evitar que o procedimento seja realizado em situações cujas chances de sucesso são claramente diminuídas.
Durante muito tempo um dos principais fatores para essa avaliação foi o tempo decorrido entre a vasectomia e o desejo por sua reversão: acreditava-se que quanto maior esse tempo fosse, menores seriam as chances de que a reversão reestabelecesse a fertilidade masculina.
O tempo realmente é um fator preponderante para o sucesso da reversão da vasectomia, porém está mais relacionado à perda natural da fertilidade, que acontece com o passar do tempo, tanto para homens quanto para mulheres, embora o homem nunca se torne infértil por causa da idade.
Outros aspectos, como a ocorrência de doenças prévias relacionadas ao sistema reprodutivo masculino, como ISTs (infecções sexualmente transmissíveis) ou traumas, a exposição a agentes gonadotóxicos, como acontece nos tratamentos oncológicos, e principalmente a presença de hidrocele também interferem nas chances de sucesso.
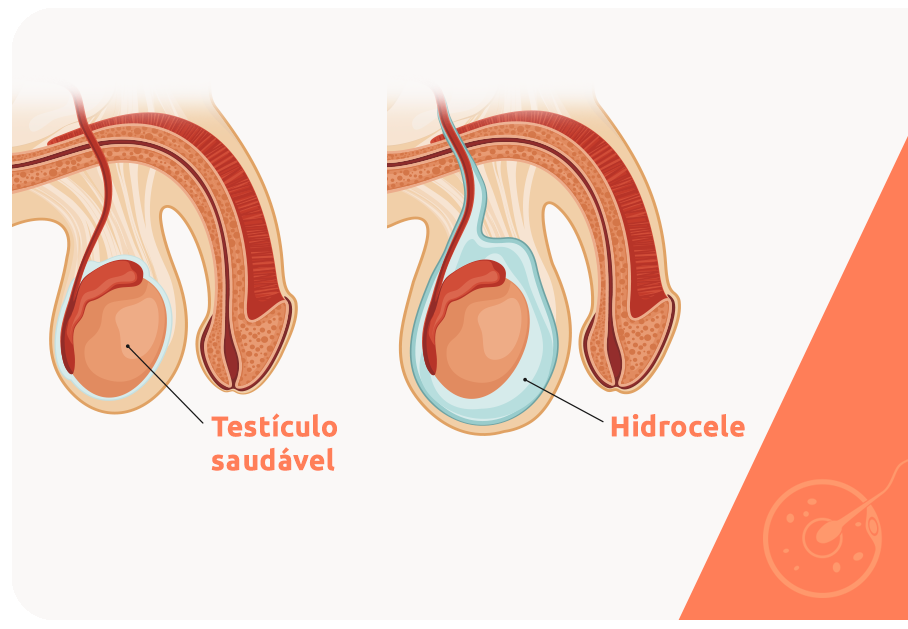
Uma das possíveis complicações da vasectomia é a hidrocele, uma reação inflamatória que provoca o acúmulo de líquido na região testicular, prejudicando a espermatogênese (formação dos espermatozoides). A presença de hidrocele é um fator que aumenta as chances de falha da reversão da vasectomia.
É importante que a fertilidade da parceira seja igualmente investigada, já que a fecundação também depende deste fator. De forma geral, podemos dizer que a reversão da vasectomia tem contraindicação relativa para casais em que a mulher tem mais de 37 anos, ou apresenta problemas de saúde relacionados a uma baixa reserva ovariana e prejuízo da função tubária.
As contraindicações para esta cirurgia referem-se aos casos em que as chances de a reversão ser bem-sucedida estão prejudicadas por problemas de saúde com efeitos diretos na espermatogênese, e também quando a parceira apresenta problemas de fertilidade, incluindo os fatores determinados pela idade.
Estes aspectos não inviabilizam a reversão da vasectomia, mas diminuem ainda mais as chances de uma gestação conseguida por vias naturais, após o procedimento.
Nesses casos, e também quando a reversão da vasectomia não dá certo, a reprodução assistida é a principal indicação para que o casal consiga ter filhos.
Dentre as técnicas de reprodução assistida disponíveis atualmente, apenas a FIV (fertilização in vitro) pode ser indicada para homens vasectomizados, por possibilitar a coleta de espermatozoides diretamente dos testículos ou epidídimos, por punção, e como a concentração e motilidade dos espermatozoides obtidos nesse procedimento são bastante reduzidas, a fecundação dos óvulos terá de ocorrer pela técnica da ICSI, utilizada em fator masculino grave.
Leia mais sobre esse assunto tocando aqui.
MaisA preservação social da fertilidade pode ser indicada para qualquer mulher, sem que obrigatoriamente existam diagnósticos prévios de infertilidade, ou para a herança de doenças genéticas.
Engravidar é um projeto que compõe o planejamento familiar de muitas mulheres, porém cada vez mais o momento de realização deste projeto tem sido adiado. Vivendo numa sociedade mais dinâmica e também mais inclusiva, as mulheres hoje se preocupam mais com a construção de suas carreiras, estabilidade financeira e a realização de outras vivências, como viagens, antes de serem mães.
No entanto, o tempo pode ser um inimigo da fertilidade feminina, já que o período reprodutivo das mulheres termina aproximadamente entre a 4ª e a 5ª décadas de vida, com a menopausa.
Por isso, a atual tendência para o adiamento da maternidade deve-se, também, ao desenvolvimento da medicina reprodutiva, que hoje permite às mulheres a preservação social da fertilidade, com o congelamento de óvulos, para serem fecundados no momento mais adequado.
Apenas a FIV (fertilização in vitro) permite a preservação social da fertilidade, já que após a coleta dos folículos, a única forma de realizar a fecundação é em ambiente laboratorial, com posterior transferência dos embriões para o útero da mulher.
A coleta de óvulos para a preservação social da fertilidade deve ser realizada a partir das primeiras etapas da FIV: estimulação ovariana e coleta por punção ovariana.
A partir desse momento, ao invés de dar continuidade ao procedimento com a fecundação, cultivo embrionário e transferência, os folículos coletados são vitrificados e armazenados.
A preservação social da fertilidade é uma técnica que pode ser utilizada por homens e mulheres, no entanto, como o período reprodutivo masculino não tem um tempo de duração tão curto, na maior parte das vezes são as mulheres que recorrem a esta ferramenta.
Este texto explica melhor como é a técnica que permite a preservação social da fertilidade e, com isso, uma melhor adequação do planejamento familiar da mulher.
A preservação social da fertilidade realiza-se a partir do congelamento dos óvulos de mulheres em idade reprodutiva, que desejam adiar a maternidade sem, com isso, ter riscos aumentados de não conseguir engravidar ou ter abortos devido à diminuição da quantidade e qualidade dos óvulos com o avançar da idade.
A preservação social da fertilidade pode ser indicada para qualquer mulher, considerando que o prognóstico é mais favorável para mulheres com boa reserva ovariana, que obterão uma boa quantidade e qualidade dos óvulos, sem que obrigatoriamente existam diagnósticos prévios de infertilidade, ou para a herança de doenças genéticas, embora a própria opção de congelar os óvulos abra espaço para procedimentos preventivos em relação a essas duas possibilidades, por estar atrelada à FIV.
Aquelas mulheres que já planejam engravidar após os 38 anos, seja por motivos profissionais, seja por motivos pessoais, o ideal seria fazer o congelamento dos óvulos até os 35 anos, já que após essa idade a reserva ovariana começa a entrar em um processo de declínio mais acelerado.
No entanto, não existe contraindicação quanto à idade em que a mulher pode realizar a preservação social da fertilidade.
Para realizar a preservação social da fertilidade a mulher deve dar início a um tratamento que inclui apenas as primeiras etapas da FIV, como mencionamos, estimulação ovariana e a aspiração folicular por punção.
A estimulação ovariana é uma etapa compartilhada por todas as técnicas de reprodução assistida, além da FIV, de forma mais intensa, – RSP (relação sexual programada) e IA (inseminação artificial) –, e consiste em potencializar o ciclo reprodutivo, com administração exógena de gonadotrofinas.
Esta etapa deve ter início entre 2 e 4 dias do ciclo reprodutivo, a partir do qual a mulher recebe doses diárias de FSH (hormônio folículo-estimulante) e LH (hormônio luteinizante), que atuam induzindo o recrutamento e crescimento dos folículos ovarianos.
A estimulação ovariana deve ser monitorada por ultrassonografia transvaginal, que acompanha todo o processo, permitindo a avaliação do crescimento dos folículos, e do melhor momento para realizar a aspiração folicular.
A aspiração dos folículos ovarianos é feita por punção ovariana, com auxílio da ultrassonografia transvaginal. As imagens são obtidas em tempo real e uma agulha específica é acoplada a um cateter, que será introduzido no canal vaginal e a aspiração se dará com auxílio de uma bomba de aspiração disposta na outra extremidade do sistema.
Os folículos antrais serão então visualizados, no monitor ligado ao ultrassom, e aspirados de forma precisa, para que este procedimento não lesione o tecido ovariano.
Para os casos em que essas etapas têm como objetivo realizar a preservação social da fertilidade, a partir da aspiração folicular, os óvulos maduros são encaminhados para o congelamento, realizado hoje por vitrificação, podendo permanecer preservados por tempo indeterminado.
Quando a mulher decide engravidar, após a preservação social da fertilidade, deve procurar a equipe médica, que realizou os procedimentos para o congelamento dos óvulos, e então dar continuidade ao tratamento com a FIV.
Antes de realizar o descongelamento dos óvulos, a mulher deve passar pelo processo de preparação endometrial, seja num ciclo natural, seja num ciclo medicado, com a administração de doses de estrogênio e progesterona.
Quando o endométrio se mostra perfeitamente preparado, com uma boa espessura evidenciada na ultrassom e com padrão trilaminar, será marcada a coleta do sêmen e no mesmo dia os óvulos serão descongelados. Nos casos em que a mulher opta por uma gestação independente, os gametas masculinos devem ser oriundos de doação – e serão descongelados também neste momento.
A vitrificação é considerada a técnica mais bem-sucedida, atualmente, para o congelamento dos óvulos, sêmen e outros materiais biológicos, pois oferece maior prevenção à formação de cristais no interior das células congeladas e, com isso, aumenta a taxa de sobrevivência dessas células.
Por isso, a realização da fecundação a partir de gametas congelados não interfere nas taxas de sucesso gerais da FIV.
Após o descongelamento, a fecundação é então realizada em ambiente laboratorial, e os embriões obtidos permanecem em fase de cultivo durante 3 a 5 dias, quando seu desenvolvimento e integridade serão avaliados.
A transferência embrionária é realizada após esse período, e aproximadamente 14 dias depois a mulher pode realizar o teste de gravidez.
Entenda melhor o que é preservação social da fertilidade tocando aqui!
MaisAlgumas doenças, como a endometriose ovariana, afetam a reserva ovariana, levando a uma diminuição precoce do potencial de fertilidade das mulheres.
A endometriose é considerada uma das doenças ginecológicas mais comuns e pode causar infertilidade, especialmente quando afeta os ovários e pode levar a uma diminuição da reserva ovariana.
A endometriose ovariana normalmente leva à formação de endometriomas, que são cistos avermelhados aderidos ao córtex do ovário, no qual estão localizadas as células reprodutivas femininas (oócitos).
A presença dos endometriomas pode aumentar a pressão sobre as glândulas sexuais femininas e alterar o equilíbrio do estrogênio, prejudicando a maturação folicular e danificando os oócitos, o que pode provocar infertilidade.
A reserva ovariana é a quantidade de folículos presentes nos ovários e pode ser avaliada por uma série de exames, que incluem dosagens hormonais, como o hormônio antimülleriano (HAM) e a inibina B, e por meio de exames de imagem, como a ultrassom endovaginal para contagem de folículos antrais (CFA).
O prejuízo causado pelos endometriomas ao amadurecimento folicular, além de gerar anovulação e/ou disovulia, também leva a uma diminuição da reserva ovariana e, consequentemente, das possibilidades de engravidar.
Este texto explica melhor como é a relação entre os endometriomas e a diminuição da reserva ovariana, apresentando tratamentos e a reprodução assistida como saída para os casos mais graves.
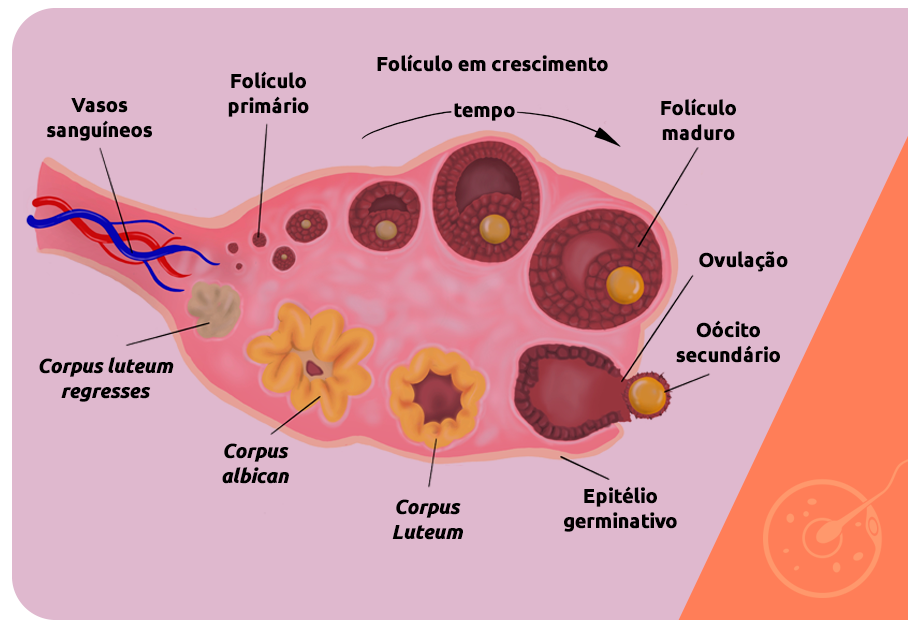
A reserva ovariana é a quantidade de folículos com potencial para ovulação, contidos nos ovários de uma mulher. A reserva ovariana surge ainda no período embrionário e até a 8ª semana de gestação já está completa; após o nascimento, no entanto, não é possível produzir mais nenhum folículo, apenas recrutar e amadurecer aqueles formados durante o desenvolvimento fetal.
Isso significa que, ao longo da vida, a reserva ovariana diminui sistematicamente e, em alguns momentos específicos, como a puberdade e o climatério, adquirem velocidades diferentes nessa diminuição.
A ovulação é um processo cíclico, por meio do qual os folículos ovarianos são recrutados, amadurecidos e rompidos para a liberação do oócito contido nele. A cada ciclo, cerca de 1000 folículos são recrutados, porém apenas um completa o processo de amadurecimento e rompimento para a liberação do óvulo, fazendo da ovulação o principal mecanismo de depleção da reserva ovariana ao longo da vida.
A partir dos 35-40 anos, a reserva ovariana apresenta um declínio mais intenso, e a fertilidade da mulher passa a declinar. Aproximadamente na 5ª década de vida, a reserva ovariana – e a função reprodutiva das mulheres – termina, o que caracteriza a menopausa.
Algumas doenças, como a endometriose ovariana, afetam a reserva ovariana, levando a uma diminuição precoce do potencial de fertilidade das mulheres.
A endometriose é uma doença crônica inflamatória de difícil diagnóstico, prevalente em até 10% da população mundial de mulheres, que pode ter consequências indesejadas para a fertilidade feminina.
Existem 3 tipos de endometriose, de acordo com a localização dos focos de endométrio ectópico, e os diferentes graus de infiltração desses focos (superficiais ou profundos) também revelam muito sobre a intensidade dos sintomas e as possibilidades de tratamento.
Os endometriomas são cistos avermelhados, formados de tecido endometrial ectópico, que se desenvolvem nos ovários, sendo estrogênio-dependentes, ou seja, seu surgimento e desenvolvimento depende da ação desse hormônio sexual, produzido durante o ciclo reprodutivo pelos ovários.
A origem da endometriose e dos endometriomas, no entanto, ainda é obscura para a medicina reprodutiva. Uma das principais teorias aceitas hoje é a teoria de Sampson ou teoria da menstruação retrógrada, que explica o surgimento de endométrio ectópico.
Essa teoria aponta o refluxo menstrual como agente disseminador do crescimento de endométrio fora do útero: por uma dificuldade de esvaziamento uterino durante a menstruação, esse tecido subiria para as tubas uterinas, caindo na cavidade abdominal, onde se implantaria e desenvolveria nos vários órgãos ali presentes, como intestino, bexiga, ovário e tubas uterinas entre outros.
No entanto, existem muitas outras teorias que buscam explicar as causas da endometriose, uma vez que ela se manifesta de formas muito variadas.
Os principais fatores de risco para endometriomas são nunca ter engravidado (nuliparidade), ter parentes próximas que já sofreram da doença, presença de malformações genitais.
O tratamento para os endometriomas deve ser indicado quando observa-se a presença de sintomas ou quando a mulher deseja engravidar.
Os principais sintomas da endometriose ovariana são irregularidades menstruais, dismenorreia, dores pélvicas e infertilidade por anovulação e/ou disovulia.
A indicação de tratamento medicamentoso é feita para as mulheres com sintomas leves e que não desejam engravidar, já que é feito com base na administração de anticoncepcionais orais combinados ou com progestagênios isolados.
Para as mulheres que desejam engravidar, o mais recomendado é a reprodução assistida, como a FIV (fertilização in vitro), porque a retirada dos endometriomas por intervenção cirúrgica tem grandes chances de prejudicar a reserva ovariana.
Quer saber mais sobre a endometriose? Toque no link!
Mais
